题目内容
7.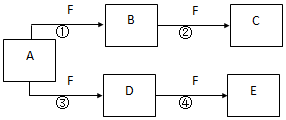 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,D的钠盐是一种致癌物质,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,D的钠盐是一种致癌物质,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:(1)Z元素的原子结构示意图
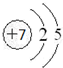 ,A的电子式为
,A的电子式为 ,
,(2)组成E的各元素的原子半径由大到小的顺序为N>O>H(用元素符号表示).
(3)写出下列反应的化学方程式:①4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;③2NH3+3O2═2HNO2+2H2O;
(4)A和E反应生成G,Z2Y是一种麻醉剂,也称为“笑气”,由G在210℃分解生成,该分解反应的化学方程式为NH4NO3$\frac{\underline{\;210℃\;}}{\;}$N2O↑+2H2O.
(5)常温下,G的水溶液的PH=5,则由水电离的氢离子浓度为10-5mol/L,离子浓度由大到小的关系c(NO3-)>c(NH4+)>c(H+)>c(OH-).
分析 X、Y、Z是三种短周期元素,Z的电子层数是X的电子层数的2倍,判断X是H元素,Z是第二周期元素.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,则A为NH3,Y、Z中有一种元素为N元素,X和Z的质子数之和与Y的质子数相等,若Y为N元素,则Z的质子数为7-1=6,则Z为C元素,结构框图转化关系可知不符合题意.若Z为N元素,则Y的质子数为1+7=8,则Y为O元素,F是一种单质,能与氨气反应,则F为O2,结合转化关系分析判断B为NO,C为NO2,D、E是两种酸,反应③④均在微生物作用下进行,D的钠盐是一种致癌物质,则D为HNO2,E为HNO3,符合题意,据此解答.
解答 解:(1)根据上面的分析可知,Z为N元素,原子结构示意图为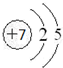 ,A为NH3,其电子式为
,A为NH3,其电子式为 ,
,
故答案为: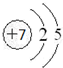 ;
; ;
;
(2)E为HNO3,组成E的各元素中,H原子半径最小,同周期原子序数越大原子半径越小,故原子半径由大到小的顺序为N>O>H,
故答案为:N>O>H;
(3)反应①的方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,反应③的方程式为:2NH3+3O2═2HNO2+2H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;2NH3+3O2═2HNO2+2H2O;
(4)A和E反应生成G为NH4NO3,Z2Y为N2O,是一种麻醉剂,由NH4NO3在210℃分解生成,根据质量守恒可知,还生成水,反应的化学方程式为:NH4NO3$\frac{\underline{\;210℃\;}}{\;}$N2O↑+2H2O,
故答案为:NH4NO3$\frac{\underline{\;210℃\;}}{\;}$N2O↑+2H2O;
(5)常温下,NH4NO3的水溶液的PH=5,溶液氢离子为水电离产生,则由水电离的氢离子浓度为10-5mol/L,溶液中NH4+水解,平衡水的电离平衡,溶液呈酸性,故离子浓度由大到小的关系c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:10-5mol/L;c(NO3-)>c(NH4+)>c(H+)>c(OH-).
点评 本题考查元素化合物推断、常用化学用语、半径比较、盐类水解等,推断元素及化合物是解题的关键,对学生的逻辑推理有一定的要求,难度中等.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案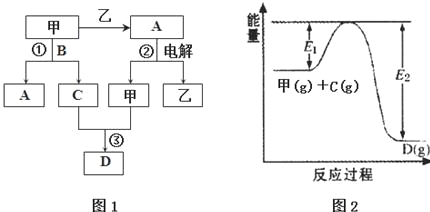
请回答下列问题:
(1)图1所示转化过程中包含的反应类型有cd(填字母).
a.置换反应 b.复分解反应c.分解反应 d.化合反应
(2)图1中反应①的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(3)图1中反应③在一定条件下为可逆反应,反应的能量变化如图2所示,当该反应处于平衡状态时,下列措施中有利于提高C的平衡转化率的是BC(填字母).
A.升高温度 B.降低温度 C.增大压强D.减小压强 E.加入催化剂 F.增加C的量
(4)若将l.00mol甲和2.00mol C混合充入容积为2L的密闭容器中,3分钟后反应达到平衡.平衡后混合气体总物质的量为2.55mol,用甲表示的化学反应速率为0.075 mol•L-1•min-1.
(5)容积均为2L的四个密闭容器中均进行着(4)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如表所示:
| 容器编号 | n(甲) | n(C) | n (D) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②? |
| Ⅲ | 0.60 | 1.20 | 0.80 | ③? |
填写表中空格:②v正<v逆 ③v正>v逆.
| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 蒸馏时,温度计的水银球应靠近蒸馏烧瓶的底部 | |
| C. | 容量瓶用水洗净后,可不经干燥直接用于配制溶液 | |
| D. | 配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
| A. | 将饱和FeCl3溶液逐滴滴加到NaOH溶液中,即可制得Fe(OH)3胶体 | |
| B. | FeCl3溶液是电中性的,Fe(OH)3胶体是带正电荷的 | |
| C. | 可利用丁达尔现象区别FeCl3溶液和Fe(OH)3胶体 | |
| D. | 将500mL 2mol/L FeCl3溶液制成胶体,胶粒的数目为NA |
| A. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.8NA | |
| D. | 标准状况下,2.24 L已烷含有分子的数目为0.1NA |
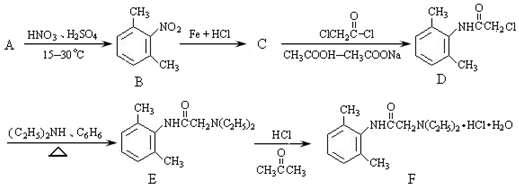
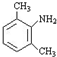 ;
;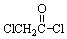 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: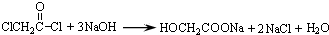 .
.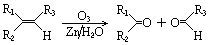
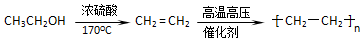
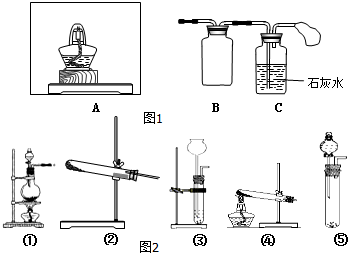 Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.
Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.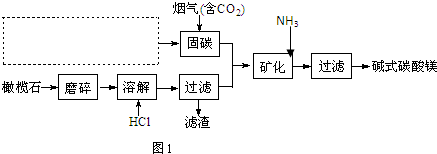
 .
.