��Ŀ����
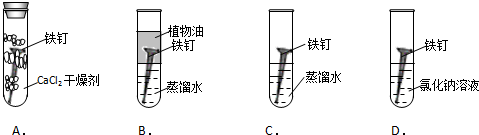
5�� С����ͼװ����ʵ��װ�ã�����ͷ�ι��еĹ���������Һ�����ȣ�Ũ�ȷֱ�Ϊ5%��10%����ʵ��ʱ��ͬʱ��ȫ������ιܵĽ�ͷ�����۲�ʵ������
С����ͼװ����ʵ��װ�ã�����ͷ�ι��еĹ���������Һ�����ȣ�Ũ�ȷֱ�Ϊ5%��10%����ʵ��ʱ��ͬʱ��ȫ������ιܵĽ�ͷ�����۲�ʵ��������1��С����ʵ��Ŀ���ǣ��Ƚ���ͬ�����������£���ͬŨ�ȡ�ͬ�������������Һ�ֽⷴӦ���ʵĴ�С�����Ũ�ȶԻ�ѧ��Ӧ�ٶȵ�Ӱ�죮
��2��װ���г��������ܵ������ǣ���ͬ��Һ������仯��ϸ���IJ�����������ɵ�Һ��߶ȱ仯���ڹ۲죻��īˮ��������ʹ�����е�Һ�����ֺ�ɫ�����ڹ۲쵼����Һ��߶ȵı仯��
��3��������������������е�ʵ����������װ���е����ڵ�Һ���������װ��B�е�����Һ��������ٶȱ�װ��A�Ŀ죻����������������ͬʱ��Ũ�ȴ�Ĺ���������Һ�ֽ����ʿ죬��λʱ���ڲ���������࣬ѹ�ϵ�Һ���߶����ߣ�
���� ��1���������⣬��ͼ��֪����������ݻ���ȣ�Ũ�Ȳ�ͬ����Ӧ���õĴ�����ͬ����ʵ��Ŀ�ģ�
��2��ϸ���IJ����ܡ���īˮ����ɫ���ڹ۲����ó�ȷ�Ľ��ۣ�
��3��˫��ˮ�ڶ��������������������·ֽ�����������Թ��ڵ�ѹǿ���������ں�īˮ������B�й��������Ũ�ȸ���Ӧ���죬����������࣮
��� �⣺��1���������⣬��ͼ��֪����������ݻ���ȣ�Ũ�Ȳ�ͬ����Ӧ���õĴ�����ͬ��֪ʵ��Ŀ��Ϊ���Ƚ���ͬ�����������£���ͬŨ�ȡ�ͬ�������������Һ�ֽⷴӦ���ʵĴ�С�����Ũ�ȶԻ�ѧ��Ӧ�ٶȵ�Ӱ�죬
�ʴ�Ϊ���Ƚ���ͬ�����������£���ͬŨ�ȡ�ͬ�������������Һ�ֽⷴӦ���ʵĴ�С�����Ũ�ȶԻ�ѧ��Ӧ�ٶȵ�Ӱ�죻
��2����ͬ��Һ������仯��ϸ���IJ�����������ɵ�Һ��߶ȱ仯��īˮ����ɫ�����ڹ۲����ó�ȷ�Ľ��ۣ��ʴ�Ϊ����ͬ��Һ������仯��ϸ���IJ�����������ɵ�Һ��߶ȱ仯���ڹ۲죻ʹ�����е�Һ�����ֺ�ɫ�����ڹ۲쵼����Һ��߶ȵı仯��
��3��˫��ˮ�ڶ��������������������·ֽ�����������Թ��ڵ�ѹǿ���������ں�īˮ������B�й��������Ũ�ȸ���Ӧ���죬��λʱ���ڲ���������࣬ѹ�ϵ�Һ���߶����ߣ�
�ʴ�Ϊ����װ���е����ڵ�Һ���������װ��B�е�����Һ��������ٶȱ�װ��A�Ŀ죻����������ͬʱ��Ũ�ȴ�Ĺ���������Һ�ֽ����ʿ죬��λʱ���ڲ���������࣬ѹ�ϵ�Һ���߶����ߣ�
���� ����̽��Ӱ�컯ѧ��Ӧ���ʵ����أ����ÿ��Ʊ����������ǽ���Ĺؼ���ע��ʵ���������������Ŀ�Ƚϼ�

 ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�| A�� | ����������̼���⡢������Ԫ����ɵĻ����� | |
| B�� | ����������2��̼ԭ�ӡ�5����ԭ�Ӻ�1����ԭ�ӹ��ɵ� | |
| C�� | �����������䶳��������е�ϵͣ��ӷ������й� | |
| D�� | ��������̼���⡢������Ԫ�ص�������Ϊ48��10��7l |
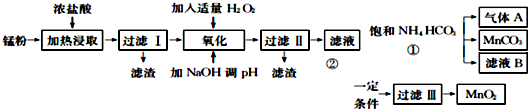
��֪�����������↑ʼ��������ȫ������pH�����
| �������� | Fe��OH�� | Fe��OH�� | Mn0H��2 | Zn��OH��2 |
| ��ʼ������pH | 7.5 | 2.2 | 8.8 | 6.4 |
| ������ȫ��pH | 9.5 | 3.7 | 10.8 | 8.5 |
��1�����˹��õ���������Ҫ�ɷ���̼�ڣ�
��2����Һ�����������NaOH��Һ����pH��8.5〜8.8����Ŀ���dz�ȥFe3+��Zn2+��
��3�����ˢ�õ�����Һ�к��е���������Ҫ��Mn2+��NH4+��Na+�������ӷ��ţ���
��4�����̢��з�����Ӧ�����ӷ���ʽΪMn2++2HCO3-=MnCO3+CO2��+H2O��������A����ҺBӦ��ȡ�Ĵ��������ֱ���CO2ѭ�����ã���������NH4HCO3����ҺB�к���NH4Cl���ɷ����������ʣ�
��5�����̢ڵõ�MnO2����MnO2������Һ��ͨS02��ԭ�ɵ�MnSO4���ټ���Na2CO3��NaHCO3��Ҳ���Ʊ�MnCO3��SO2��ԭMnO2�Ļ�ѧ����ʽΪMnO2+S02=MnSO4����MnS04��Һ�м���Na2C03��NaHC03�Ʊ�MnC03ʱӦע��������DZ߽������Na2C03��NaHC03����������Һ��pH��8.8��

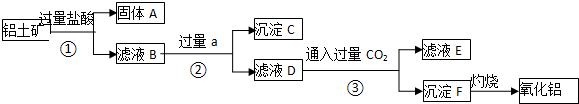
 ijѧ������ͼ��ʾװ�ý��л�ѧ��ӦX+2Y�T2Z�����仯������о��������Թ��еμ��Լ�Yʱ�����������м״�Һ���½����Ҵ�Һ�����������ڸ÷�Ӧ��������ȷ���ǣ�������
ijѧ������ͼ��ʾװ�ý��л�ѧ��ӦX+2Y�T2Z�����仯������о��������Թ��еμ��Լ�Yʱ�����������м״�Һ���½����Ҵ�Һ�����������ڸ÷�Ӧ��������ȷ���ǣ������� 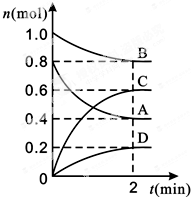 T��ʱ�����ݻ�Ϊ0.5L���ܱ������з���ijһ��Ӧ���Ҳ�ò�ͬʱ����������������A��B��C��D�����ʵ����仯��ͼ��ʾ����֪������A��B��C��Ϊ��̬��DΪ��̬������Ӧ�����ȷ�Ӧ������Ҫ��ش��������⣺
T��ʱ�����ݻ�Ϊ0.5L���ܱ������з���ijһ��Ӧ���Ҳ�ò�ͬʱ����������������A��B��C��D�����ʵ����仯��ͼ��ʾ����֪������A��B��C��Ϊ��̬��DΪ��̬������Ӧ�����ȷ�Ӧ������Ҫ��ش��������⣺