题目内容
11.下列离子方程式书写正确的是( )| A. | Na2O2 与H2O反应制备O2 :2Na2O2 +2H2O═4Na++4OH-+O2↑ | |
| B. | Cl2通入石灰乳中:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 氢氧化钠溶液腐蚀玻璃:2OH-+SiO2═SiO32-+H2O |
分析 A.反应生成NaOH和氧气,遵循电子、电荷守恒;
B.石灰乳为氢氧化钙,在离子反应中保留化学式;
C.反应生成氢氧化铝和氯化铵;
D.二氧化硅与NaOH反应生成硅酸钠和水.
解答 解:A.Na2O2 与H2O反应制备O2 的离子反应为2Na2O2 +2H2O═4Na++4OH-+O2↑,故A正确;
B.Cl2通入石灰乳中的离子反应为Cl2+2Ca(OH)2═2Ca2++Cl-+ClO-+H2O,故B错误;
C.AlCl3溶液中加入过量稀氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C错误;
D.氢氧化钠溶液腐蚀玻璃的离子反应为2OH-+SiO2═SiO32-+H2O,故D正确;
故选AD.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,选项B为解答的难点,题目难度不大.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
2.下列叙述不正确的是( )
| A. | 4.6 gNa与O2完全反应,生成7g产物时失去电子的物质的量为0.2 mol | |
| B. | Na与稀硫酸反应的离子方程式为2Na+2H+=2Na++H2↑ | |
| C. | 将少量Na投入到CuSO4溶液中,既有沉淀生成又有气体放出 | |
| D. | 金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
3.最早总结出元素周期律,画出元素周期表的科学家是( )
| A. | 道尔顿 | B. | 阿伏加德罗 | C. | 门捷列夫 | D. | 普里斯特利 |
6.已知反应: +
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$ 如果要合成化合物A,其结构为:
如果要合成化合物A,其结构为: 下列说法不正确的是( )
下列说法不正确的是( )
 +
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$ 如果要合成化合物A,其结构为:
如果要合成化合物A,其结构为: 下列说法不正确的是( )
下列说法不正确的是( )| A. | 化合物A和HBr 按照物质的量1:1加成时,有三种不同的产物 | |
| B. | 该反应的原理是加成反应 | |
| C. | 合成A的原料可能是:丙炔和2,3-二甲基-1,3-丁二烯 | |
| D. | 合成A的原料可能是:2-丁炔和2-甲基-1,3-丁二烯 |
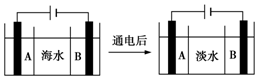 水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.
水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源. .它位于元素周期表的第三周期,第ⅢA族.
.它位于元素周期表的第三周期,第ⅢA族.