题目内容
17.下列离子方程式或说法正确的是( )| A. | 向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:6I-+8H++2NO3-=3I2+4H2O+2NO↑ | |
| B. | 非金属元素形成的化合物一定是共价化合物 | |
| C. | SO2通入Ca(ClO)2溶液中:SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO | |
| D. | 只含有共价键的物质一定是共价化合物 |
分析 A.碘离子、二价铁离子都具有还原性,氢离子少量,碘离子先被氧化;
B.氯化铵为离子化合物;
C.少量SO2通入Ca(ClO)2溶液中,发生氧化还原反应生成硫酸钙;
D.只含有共价键的物质可能共价化合物,也可能是非金属单质如H2.
解答 解:A.在酸性溶液中NO3-具有氧化性,由于I-的还原性强于Fe2+的,所以首先氧化的是I-,离子方程式:6I-+8H++2NO3-=3I2+4H2O+2NO↑,故A正确;
B.非金属元素形成的化合物不一定是共价化合物,例如氯化铵,为离子化合物,故B错误;
C.少量SO2通入Ca(ClO)2溶液中的离子反应为SO2+Ca2++ClO-+H2O=CaSO4↓+2H++Cl-,故C错误;
D.只含有共价键的物质可能共价化合物,也可能是非金属单质如H2,故D错误;
故选:A.
点评 本题考查了离子方程式、化学方程式的书写正误判断,明确反应实质是解题关键,注意反应物用量对反应的影响,注意离子还原性强弱顺序,题目难度中等.

练习册系列答案
相关题目
5.《化学反应原理》一书中,我们学习了两个重要的定量实验.请回答下列问题:
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q(放)=C m(t2-t1),反应后溶液的比热容C为4.18KJ?℃-1?Kg-1,m指溶液的质量,各物质的密度均为1g?cm-3.
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
(i)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-.
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 试剂如下: | 溶 液 温 度 | 中和热△H | ||||
| t1 | t2 | |||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | ||
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | ||
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
12.某均匀混合的白色粉末可能含有下列7种常见物质中的某4种:NaCl、BaCl2、Mg(NO3)2、K2CO3、CuSO4、NaHCO3、X,混合物中各成分的物质的量相等,且所含阴、阳离子数目之比为3:2,某同学做了以下实验,部分现象没有描述.根据所提供的实验现象,下列对该白色粉末的判断正确的是( )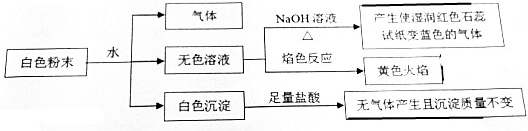

| A. | 一定含有BaCl2、Mg(NO3)2、NaHCO3、X,且X是NH4HSO4 | |
| B. | 一定不含K2CO3、CuSO4,X是NH4Al(SO4)2 | |
| C. | 一定含有BaCl2、NaHCO3、X且X是NH4AlO2,另一种为NaCl和Mg(NO3)2中的任一种 | |
| D. | 一定含有NaCl、BaCl2、NaHCO3和X,当X不能确定是什么物质 |
2.要除去氯化亚铁溶液中的少量氯化铁,可行的办法是( )
| A. | 滴入KSCN溶液 | B. | 通入氯气 | C. | 滴入NaOH溶液 | D. | 加入铁粉 |
6.下列有关同分异构体数目的叙述中,正确的是( )
| A. | 甲苯苯环上的一个氢原子被含 4 个碳原子的烷基取代,所得产物有12种 | |
| B. | 等物质的量的氯气与乙烷在光照条件下反应得到10种产物 | |
| C. | 已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为6种 | |
| D. | 苯乙烯和氢气完全加成的产物的一溴取代物有5种 |
7.下列有关叙述正确的是( )
| A. | 银锌纽扣电池工作时,Ag2O被还原为Ag | |
| B. | 碱性锌锰电池中,MnO2是催化剂 | |
| C. | 放电时,铅酸蓄电池中硫酸浓度不断增大 | |
| D. | 电镀时,待镀的金属制品表面发生还原反应 |
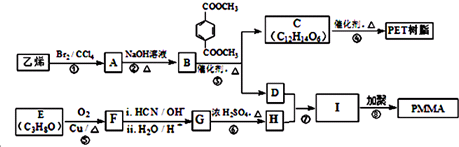
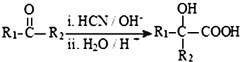 (R、R1、R2、R3均代表烃基)
(R、R1、R2、R3均代表烃基)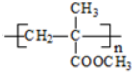 .
.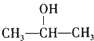 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2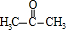 +2H2O.
+2H2O.