题目内容
9.0.2molCO(NH2)2(尿素)中含0.8mol氢原子,所含碳元素的质量是2.4g,含0.4NA个氮原子.分析 依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$,结合尿素分子的构成解答.
解答 解:依据尿素分子式CO(NH2)2可知;1个尿素分子中含有4个H,2个N,1个C,则:0.2molCO(NH2)2(尿素)含有氢原子物质的量为0.2mol×4=0.8mol;含有碳元素的质量为:0.2mol×1×12g/mol=2.4g;含有氮原子数目为:0.2mol×2×NA=0.4NA,
故答案为:0.8,2.4,0.4NA.
点评 本题考查了物质的量有关计算,明确以物质的量为核心的计算公式及尿素分子的构成是解题关键,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
17.下列说法中正确的是( )
| A. | 1mol纯物质完全燃烧时所放出的热量叫做该物质的燃烧热 | |
| B. | 对于任何化学反应,反应的速率越大,反应现象越明显 | |
| C. | SO2溶于水能导电,所以SO2是电解质 | |
| D. | 某溶液的pH=7,则该溶液不一定为中性 |
1.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 100mL 1mol/LFeCl3溶液中含有0.1NA个Fe3+ | |
| B. | 1.06g Na2CO3含有的CO32-离子数小于0.01 NA | |
| C. | PH=3的醋酸溶液中,含有的H+数为0.001NA | |
| D. | 2L 0.5mol/L的氨水中,含有NH3•H2O、NH4+、NH3的总数为1 NA |
19.某溶液中只可能含有下列离子中的几种:K+、NO3-、SO42-、NH4+、CO32-(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
| A. | 该溶液中可能含K+ | |
| B. | 该溶液中肯定含有NO3-、SO42-、NH4+、CO32- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含K+,且c(K+)≥0.1mol/L |
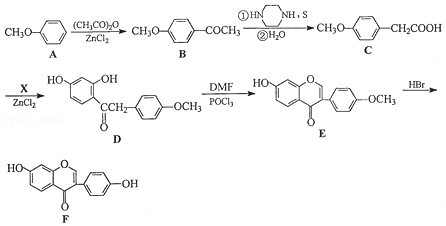
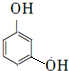 .
.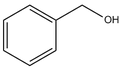 .
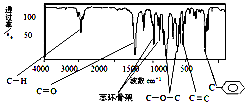
.
 (不考虑立体异构)
(不考虑立体异构)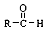 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$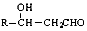 $\stackrel{-H_{2}O}{→}$RCH=CHCHO
$\stackrel{-H_{2}O}{→}$RCH=CHCHO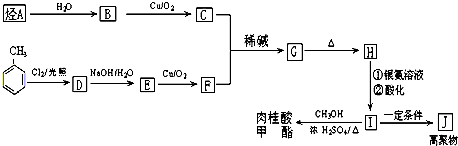

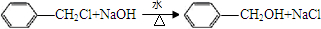
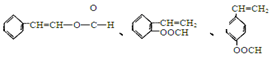
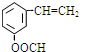 、
、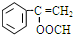 .
. 某兴趣小组设计了如图所示的原电池,请结合图中信息回答下列问题:
某兴趣小组设计了如图所示的原电池,请结合图中信息回答下列问题: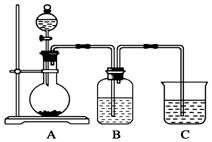 某同学设计实验以探究元素性质的递变规律,实验装置如图所示.
某同学设计实验以探究元素性质的递变规律,实验装置如图所示.