题目内容
19.将浓硫酸慢慢滴加到浓盐酸中,会产生白雾,不能解释这一现象的是( )| A. | 浓盐酸具有挥发性 | B. | 浓硫酸具有脱水性 | ||
| C. | 浓硫酸和浓盐酸中的水作用而放热 | D. | 浓硫酸有吸水性 |
分析 浓硫酸的稀释过程是一个放热过程,浓硫酸具有吸水性,浓盐酸具有挥发性,挥发出的HCl遇水蒸气形成盐酸小液滴,以此解答该题.
解答 解:浓硫酸具有吸水性,浓硫酸的稀释过程是一个放热过程,浓盐酸具有挥发性,挥发出的HCl遇水蒸气形成盐酸小液滴而产生白雾,将浓硫酸倒入浓盐酸中,相当于浓硫酸稀释,放出的热量促进浓盐酸挥发,挥发出的HCl遇空气中的水蒸气而产生白雾,浓硫酸稀释放出的热量导致混合物温度升高,与浓硫酸的脱水性无关.
故选B.
点评 本题考查浓硫酸、浓盐酸性质,为高频考点,明确浓盐酸的挥发性、浓硫酸稀释放热是解本题关键,注意烟和雾的区别,题目难度不大.

练习册系列答案
相关题目
9.在盛有溴水的试管中,加入少量苯后振荡,静置后( )
| A. | 整个溶液变橙色 | B. | 整个溶液变浅棕色 | ||
| C. | 上层无色、下层橙色 | D. | 下层无色、上层橙色 |
7.下列化合物不能由两种单质直接化合生成的是( )
①FeS ②CuS ③SO2 ④SO3.
①FeS ②CuS ③SO2 ④SO3.
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
4.能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶溶液加以区别的一种试剂是( )
| A. | Ba(OH)2 | B. | BaCl2 | C. | Ba(NO3)2 | D. | NaOH |
3.化学与生活密切相关,下列物质的化学性质与其实际应用相对应的是( )
| 选项 | 化学性质 | 实际应用 |
| A | Na、K均是活泼金属 | 钠钾合金用作原子反应堆导热剂 |
| B | H2O2能使蛋白质变性 | 医疗上用于伤口消毒 |
| C | CH2=CH2能与H2O发生加成反应 | 乙烯用作果实的催熟剂 |
| D | NH3具有还原性 | 作食品加工的制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
4.用NA为阿伏伽德罗常数的数值,下列叙述正确的是( )
| A. | 1mol/L氯化铜溶液中的Cu2+数小于NA | |
| B. | 28 g聚乙烯含有的碳原子数为2NA | |
| C. | 标准状况下,22.4 L Cl2与水反应转移的电子数为NA | |
| D. | 惰性电极电解食盐水,若线路中通过2NA电子电量,则阳极产生气体22.4L |
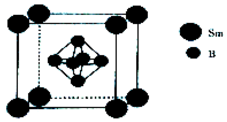 硼及其化合物在工农业生产中应用广泛.
硼及其化合物在工农业生产中应用广泛.