题目内容
19.下列有关性质的比较,不能用元素周期律解释的是( )| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:Cl>Br | ||
| C. | 碱性:热稳定性:Na2CO3>NaHCO3 | D. | NaOH>Mg(OH)2 |
分析 A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.同主族元素从上到下非金属性依次减弱;
C.碳酸氢盐易分解,碳酸盐难分解;
D.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强.
解答 解:A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,非金属性:S>P,则酸性:H2SO4>H3PO4,能用元素周期律解释,故A不选;
B.同主族元素从上到下非金属性依次减弱,则非金属性:Cl>Br,能用元素周期律解释,故B不选;
C.碳酸氢盐易分解,碳酸盐难分解,所以热稳定性:Na2CO3>NaHCO3,不能用元素周期律解释,故C选;
D.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,金属性:Na>Mg,则碱性:NaOH>Mg(OH)2,能用元素周期律解释,故D不选;
故选C.
点评 本题考查了元素周期律的理解与应用,注意把握元素周期律的递变规律以及相关知识的积累,难度不大.

练习册系列答案
相关题目
9.下列说法错误的是( )
| A. | I的原子半径大于Br,HI比HBr的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | 与水或者酸反应的剧烈程度:K>Na>Mg |
10.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),如图:下列判断错误的是( )
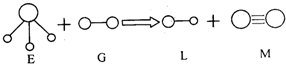
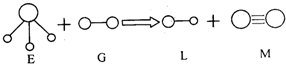
| A. | G是最活泼的非金属单质 | B. | L能使紫色石蕊试液变红色 | ||
| C. | E能使紫色石蕊试液变蓝色 | D. | M是化学性质很活泼的单质 |
14.自然界中的能源可以分为一次能源和二次能源,一次能源是指直接取自自然界没有经过加工转换的各种能量和资源,由一次能源经过加工转换以后得到的能源产品,称为二次能源.下列叙述正确的是( )
| A. | 电能是二次能源 | B. | 水力是二次能源 | ||
| C. | 天然气是二次能源 | D. | 水煤气是一次能源 |
11.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 9.2克甲苯含有的C-H数目为0.8NA | |
| B. | 1 mol羟基所含的电子数为7NA | |
| C. | 1 mol乙醇催化氧化生成乙醛时转移的电子数为4NA | |
| D. | 分子式为C3H6的有机物一定含有NA个碳碳双键 |
8.下列元素属于第三周期的是( )
| A. | 氢 | B. | 氧 | C. | 氯 | D. | 碘 |
9.下列家庭垃圾中适合于堆肥的是( )
| A. | 破旧的衣物 | B. | 瓜果壳 | C. | 废电池 | D. | 塑料瓶 |