题目内容
13.下列说法正确的是( )| A. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| B. | 实验室制备硝基苯,将苯和浓硝酸混合后加热即可 | |
| C. | 棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O | |
| D. | 1mol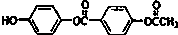 与足量的NaOH溶液加热充分反应,能消耗5molNaOH 与足量的NaOH溶液加热充分反应,能消耗5molNaOH |
分析 A、结构相似,分子组成上相差1个或n个-CH2原子团的化合物互为同系物;
B、制备硝基苯,需要浓硫酸作催化剂和吸水剂,且需要水浴加热;
C、蛋白质是由C、H、O、N、S、P等组成的化合物,燃烧产物不仅仅只有二氧化碳和水;
D、苯酚与羧酸都能与碱反应,且水解后产物中共有3个酚羟基、2个羧基.
解答 解:A、CH4O与C2H6O均为醇类时,结构相似,分子组成上一个-CH2,互为同系物,但是C2H6O可以表示甲醚,此时与甲醇不是同系物,故A错误;
B、制备硝基苯,需要浓硫酸作催化剂和吸水剂,则实验操作中缺少浓硫酸,且需要水浴加热,不能直接加热,故B错误;
C、蛋白质的燃烧产物含有S的氧化物与N的氧化物或氮气等,故C错误;
D、苯酚与羧酸都能与碱反应,且水解后产物中共有3个酚羟基、2个羧基,1mol 与足量的NaOH溶液加热充分反应,能消耗5molNaOH,故D正确;故选D.
与足量的NaOH溶液加热充分反应,能消耗5molNaOH,故D正确;故选D.
点评 本题考查有机物的结构和性质,题目难度中等,易错点为D,注意把握有机物官能团的性质,选项C中掌握蛋白质的组成是关键.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
3.实验测得BeCl2为共价化合物,两个Be-Cl键间的夹角为180°,以下判断正确的是( )
| A. | 由极性键构成的极性分子 | B. | 由极性键构成的非极性分子 | ||
| C. | 由非极性键构成的极性分子 | D. | BeCl2中Be采取sp2杂化 |
4.化学与生产、生活密切相关.下列有关叙述正确的是( )
| A. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| B. | 通过干馏可将煤中含有的苯、甲苯等物质分离出来 | |
| C. | 地沟油通过水解反应可得到车用汽油 | |
| D. | 家庭用洁厕灵与“84消毒液”不能同时使用 |
1.A、B、C、D、E五种短周期元素的原子序数依次增大,A和D、C和E分别同主族,E的原子序数为C的两倍,B的最外层电子数为A的最外层电子数的4倍.下列叙述正确的是( )
| A. | A、B、C三种元素形成的化合物一定是非电解质 | |
| B. | A与C只能形成化学式为A2C的化合物 | |
| C. | 第三周期中,D的原子半径最大 | |
| D. | E的氧化物对应的水化物一定具有强氧化性 |
5.下表为元素周期表的一部分,参照元素①~⑨在表中的位置,按要求回答下列问题:
(1)在标号元素中,最活泼的金属元素名称是钠最活泼的非金属元素名称是氟.
⑨元素的原子结构简示意图 .
.
(2)用电子式表示 ①与②形成共价化合物的形成过程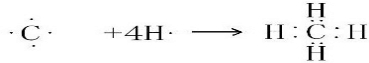 .
.
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是⑤>⑥>⑦(序号表示).
(4)①~⑨元素所形成的气态氢化物中,最稳定的是HF(化学式表示)
⑦、⑧、⑨三种元素的气态氢化物的稳定由强到弱的顺序HCl>PH3>SiH4(化学式表示).
(5)写出元素⑨的单质与溴化钠反应的离子方程式:2Br-+Cl2=2Cl-+Br2.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
⑨元素的原子结构简示意图
 .
.(2)用电子式表示 ①与②形成共价化合物的形成过程
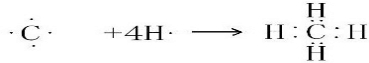 .
.(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是⑤>⑥>⑦(序号表示).
(4)①~⑨元素所形成的气态氢化物中,最稳定的是HF(化学式表示)
⑦、⑧、⑨三种元素的气态氢化物的稳定由强到弱的顺序HCl>PH3>SiH4(化学式表示).
(5)写出元素⑨的单质与溴化钠反应的离子方程式:2Br-+Cl2=2Cl-+Br2.
2.A、B是相对分子量不相等的两种有机物,无论A、B以何种比例混合,只要混合物的总质量不变,完全燃烧后生成CO2的质量也不变.符合这一条件的组合是( )
| A. | HCHO CH3COOH | B. | HCOOCH3 CH3COOH | ||
| C. | C2H4 C2H5OH | D. | CH3OH C10H8O2 |
3.元素性质呈现周期性变化的根本原因是( )
| A. | 元素的原子量逐渐增大 | B. | 核外电子排布呈周期性变化 | ||
| C. | 核电荷数逐渐增大 | D. | 元素化合价呈周期性变化 |
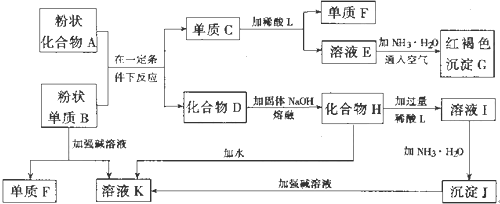
 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: