题目内容
为满足人们生活和生产的实际用水需要,必须对水进行处理,以除掉水中的悬浮物,读题回答下列问题:
(1)可用明矾除去水中的悬浮物,写出明矾在水中的电离方程式 .
(2)饮用水的杀菌、曾广泛采用液氯作消毒剂.
用液氯可制得漂粉精,写出该反应的化学方程式: .
(1)可用明矾除去水中的悬浮物,写出明矾在水中的电离方程式
(2)饮用水的杀菌、曾广泛采用液氯作消毒剂.
用液氯可制得漂粉精,写出该反应的化学方程式:
考点:化学方程式的书写,电离方程式的书写
专题:
分析:(1)明矾是强电解质,在水溶液里电离生成钾离子、铝离子和硫酸根离子,铝离子水解生成的氢氧化铝胶体能净水;
(2)氯气和石灰乳反应生成氯化钙、次氯酸钙和水,漂粉精的有效成分是次氯酸钙.
(2)氯气和石灰乳反应生成氯化钙、次氯酸钙和水,漂粉精的有效成分是次氯酸钙.
解答:
解:(1)明矾是强电解质,在水溶液里电离生成钾离子、铝离子和硫酸根离子,电离方程式为KAl(SO4)2=K++Al3++2SO42-,铝离子水解生成的氢氧化铝胶体能净水,故答案为:KAl(SO4)2=K++Al3++2SO42-;
(2)氯气和石灰乳反应生成氯化钙、次氯酸钙和水,反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂粉精的有效成分是次氯酸钙,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(2)氯气和石灰乳反应生成氯化钙、次氯酸钙和水,反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂粉精的有效成分是次氯酸钙,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评:本题考查电离方程式及化学方程式的书写,明确物质性质即可解答,注意强弱电解质电离方程式的区别,知道漂粉精的主要成分和有效成分的区别.

练习册系列答案
相关题目
常温下,将0.1mol?L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
| A、溶液的pH增加 |
| B、CH3COOH电离度变大 |
| C、溶液的导电能力减弱 |
| D、溶液中c(OH-)减小 |
除去混在碳酸钠粉末中的少量碳酸氢钠,最合理的方法是( )
| A、加盐酸 | B、加水 |
| C、加热 | D、加NaOH溶液 |
下列有关工业生产的叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率 |
| B、从海水中提镁过程中,电解熔融MgO可制备Mg |
| C、电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下: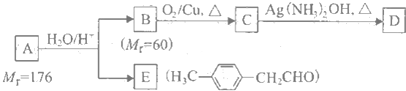
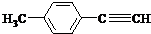 )的一条路线如下:
)的一条路线如下: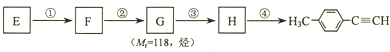
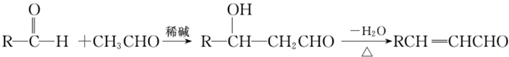
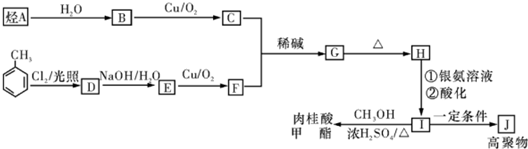
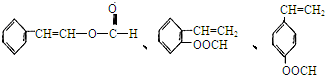 、
、