题目内容
下列有关工业生产的叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率 |
| B、从海水中提镁过程中,电解熔融MgO可制备Mg |
| C、电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
考点:工业合成氨,电解原理,海水资源及其综合利用
专题:化学应用
分析:A、减小生成物的浓度会导致化学反应速率减慢,化学平衡正向移动;
B、根据MgO比MgCl2熔点高,电解MgO比电解MgCl2的电能多分析;
C、电解精炼铜时,在阳极上是金属锌、铁、镍先于金属铜放电;
D、电解饱和食盐水时,在阴极上产生的是氢气和氢氧化钠.
B、根据MgO比MgCl2熔点高,电解MgO比电解MgCl2的电能多分析;
C、电解精炼铜时,在阳极上是金属锌、铁、镍先于金属铜放电;
D、电解饱和食盐水时,在阴极上产生的是氢气和氢氧化钠.
解答:
解:A、合成氨生产过程中将NH3液化分离,减小氨气的浓度会导致正化学反应速率减慢,化学平衡向右移动,提高N2、H2的转化率,故A正确;
B、MgO比MgCl2熔点高,电解MgO比电解MgCl2的电能多,浪费资源,所以工业上通过电解熔融氯化镁获得金属镁,故B错误;
C、电解精炼铜时,在阳极上是金属锌、铁、镍先失去电子,在阴极上是铜离子得电子生成金属Cu的过程,同一时间内阳极溶解铜的质量比阴极析出铜的质量小,溶液中铜离子浓度减小,故C正确;
D、电解饱和食盐水时,在阴极上产生的是氢气和氢氧化钠,在阳极上产生的是氯气,采用离子交换膜法,可防止阳极室产生的C12进入阴极室,故D错误;
故选AC.
B、MgO比MgCl2熔点高,电解MgO比电解MgCl2的电能多,浪费资源,所以工业上通过电解熔融氯化镁获得金属镁,故B错误;
C、电解精炼铜时,在阳极上是金属锌、铁、镍先失去电子,在阴极上是铜离子得电子生成金属Cu的过程,同一时间内阳极溶解铜的质量比阴极析出铜的质量小,溶液中铜离子浓度减小,故C正确;
D、电解饱和食盐水时,在阴极上产生的是氢气和氢氧化钠,在阳极上产生的是氯气,采用离子交换膜法,可防止阳极室产生的C12进入阴极室,故D错误;
故选AC.
点评:本题考查了工业合成氨、海水资源的应用、电解原理等知识,题目难度中等,试题综合性强,知识点较多,是一道综合知识的考查题,实际化学反应速率和化学平衡的移动的影响因素、电解精炼铜的原理等方面知识.

练习册系列答案
相关题目
某固体化合物A不导电,但熔化或溶于水都能完全电离,下列关于A的说法中正确的是( )
| A、A为非电解质 |
| B、A是强电解质 |
| C、A是分子晶体 |
| D、A为弱电解质 |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是( )
A、氢气、CO合成甲醇:2H2+CO
| ||
B、烯烃与水煤气发生反应:RCH=CH2+CO+H2
| ||
| C、CH4与Cl2反应制取CCl4 | ||
| D、氯乙烯合成聚氯乙烯 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述不正确的是( )
| A、油脂水解的产物是水和CO2 |
| B、油脂水解可得到丙三醇 |
| C、淀粉水解的最终产物是葡萄糖 |
| D、蛋白质水解的最终产物是氨基酸 |


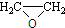 ).写出以邻甲基苯酚(
).写出以邻甲基苯酚(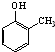 )和乙醇为原料制备
)和乙醇为原料制备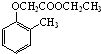 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).