题目内容
 甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.
甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.(1)以CH4和H2O为原料,通过下列反应可制备甲醇.
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.0kJ?mol-1
②CO(g)+2H2(g)?CH3OH (g)△H=-129.0kJ?mol-1
则CH4(g)+H2O(g)?CH3OH (g)+H2(g)的△H=
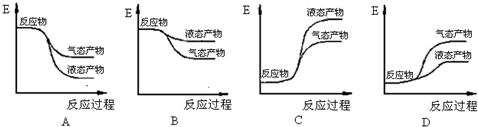
(2)将1.0mol CH4(g)和2.0mol H2O(g)通入容积为10L的容器,在一定条件下发生反应①,测得在一定压强下CH4的转化率与温度的关系如图1,设100℃时达到平衡所需的时间为5min,则这时间段v(H2)=
(3)在一定温度下,将一定量CO和H2充入密闭容器发生反应②,达到平衡后,若压缩容器体积至原的
| 1 |
| 2 |
①c(H2)减小 ②CH3OH 的物质的量增加 ③新平衡时,
| c(H2) |
| c(CH3OH) |
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).
现用如图2装置模拟上述过程,则:Co2+在阳极的电极反应式为
②请完成除去甲醇的离子方程式:
考点:转化率随温度、压强的变化曲线,用盖斯定律进行有关反应热的计算,化学平衡的影响因素,电解原理
专题:
分析:(1)根据盖斯定律来分析;
(2)列三段式表示各物质起始量、转化量、平衡量;依据反应速率计算公式V=
计算解答;
(3)其他条件不变,平衡后将容器的容积压缩到原来的
,压强增大,正、逆反应速率都增大,但正反应速率增大更多,平衡向正反应方向移动,生成物的浓度增大,由于温度不变,则平衡常数不变,结合平衡常数可知,平衡时反应物各组分的浓度都增大,据此分析解答;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,原子守恒与电荷守恒可知,还原生成H+,配平书写为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
(2)列三段式表示各物质起始量、转化量、平衡量;依据反应速率计算公式V=
| △C |
| △t |
(3)其他条件不变,平衡后将容器的容积压缩到原来的
| 1 |
| 2 |
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,原子守恒与电荷守恒可知,还原生成H+,配平书写为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
解答:
解:(1)已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.0kJ?mol-1
②CO(g)+2H2(g)?CH3OH (g)△H=-129.0kJ?mol-1
将①+②可得:CH4(g)+H2O(g)?CH3OH (g)+H2(g)的△H=(+206.0KJ/mol)+(-129.0KJ/mol)=-77KJ/mol,故答案为:-77;
(2)将1.0mol CH4和2.0mol H2O ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲烷转化率为50%,故参加反应的甲烷为1mol×50%=0.5mol,则:
CH4 (g)+H2O (g)=CO (g)+3H2 (g)
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 1.5 0.5 1.5
假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平衡反应速率V(H2)=
=0.03 mol?L-1?min-1,
故答案为:0.03 mol?L-1?min-1;
(3)在一定条件下,将一定量的CO和氢气的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,CO(g)+2H2(g)=CH3OH(g)△H=-129.0kJ/mol;
平衡后将容器的容积压缩到原来的
,其他条件不变,体积减小压强增大,反应速率增大,平衡正向进行.
①体积减小,c(H2)增大,故A错误;
②体积减小,压强增大,平衡正向进行,CH3OH的物质的量增加,故正确;
③体积减小,压强增大,平衡正向进行,重新平衡时c(H2)/c(CH3OH)减小,故正确;
④压强增大,正逆反应速率都加快,故错误;
⑤平衡常数K只随温度的而变化,故错误
故选②③;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,结合原子守恒与电荷守恒可知,还原生成H+,配平书写离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
故答案为:Co2+-e-=Co3+;6,H2O,6.
②CO(g)+2H2(g)?CH3OH (g)△H=-129.0kJ?mol-1
将①+②可得:CH4(g)+H2O(g)?CH3OH (g)+H2(g)的△H=(+206.0KJ/mol)+(-129.0KJ/mol)=-77KJ/mol,故答案为:-77;
(2)将1.0mol CH4和2.0mol H2O ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲烷转化率为50%,故参加反应的甲烷为1mol×50%=0.5mol,则:
CH4 (g)+H2O (g)=CO (g)+3H2 (g)
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 1.5 0.5 1.5
假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平衡反应速率V(H2)=
| ||
| 5min |
故答案为:0.03 mol?L-1?min-1;
(3)在一定条件下,将一定量的CO和氢气的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,CO(g)+2H2(g)=CH3OH(g)△H=-129.0kJ/mol;
平衡后将容器的容积压缩到原来的
| 1 |
| 2 |
①体积减小,c(H2)增大,故A错误;
②体积减小,压强增大,平衡正向进行,CH3OH的物质的量增加,故正确;
③体积减小,压强增大,平衡正向进行,重新平衡时c(H2)/c(CH3OH)减小,故正确;
④压强增大,正逆反应速率都加快,故错误;
⑤平衡常数K只随温度的而变化,故错误
故选②③;
(4)通电后,将Co2+氧化成Co3+,电解池中阳极失电子发生氧化反应,电极反应为Co2+-e-=Co3+;
以Co3+做氧化剂把水中的甲醇氧化成CO2而净化,自身被还原为Co2+,结合原子守恒与电荷守恒可知,还原生成H+,配平书写离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
故答案为:Co2+-e-=Co3+;6,H2O,6.
点评:本题考查热化学方程式书写、化学平衡图象、影响化学平衡因素、平衡常数与反应速率计算、原电池等,掌握基础是解本题的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质的名称、俗名与化学式完全对应的是( )
| A、氯化钠 食盐 NaCl2 |
| B、碳酸氢钠 纯碱 NaHCO3 |
| C、氢氧化钙 熟石灰 CaO |
| D、氢氧化钠 烧碱 NaOH |
在容积固定的密闭容器中发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、从700℃到900℃,平衡体系中气体的密度变大 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |
利用如图装置电解饱和食盐水,下列说法正确的是( )
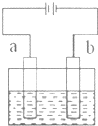

| A、b电极上发生氧化反应 |
| B、该装置能将化学能转变成电能 |
| C、电解质溶液中Cl-向a电极迁移 |
| D、若b为铁,则b电极的反应式为:Fe-2e-═Fe2+ |
下列实验结论正确的是( )
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定不含K+ |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是SO2 |
| D、向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
下列说法不正确的是( )
| A、丙烯和丙烷可用Br2的CCl4溶液来区别 |
| B、淀粉水解的最终产物是葡萄糖 |
| C、米酒变酸的过程涉及了氧化反应 |
| D、石油分馏和石油的裂化都属于化学变化 |
 可简写为
可简写为 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: