题目内容
4.人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实的分析正确的是( )| A. | 亚硝酸盐是还原剂 | B. | 维生素C是氧化剂 | ||
| C. | 维生素C将Fe3+还原为Fe2+ | D. | 亚硝酸盐被氧化 |
分析 由题给信息可知Fe2+转化为Fe3+而中毒,服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+.
解答 解:服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+,Fe元素化合价降低,被氧化,则维生素具有还原性,而亚硝酸盐,会导致Fe2+转化为Fe3+,说明亚硝酸盐具有氧化性,被还原,在反应中为氧化剂,
故选C.
点评 本题考查氧化还原反应知识,题目难度不大,注意从元素化合价的变化的角度判断物质在反应中体现的性质,答题时注意审题.

练习册系列答案
相关题目
14.W、X、Y、Z、M、Q六种短周期元素在元素周期表中的相对位置如图所示,W是形成化合物种类最多的元素,由此可知( )
| W | X | Y | ||
| Z | M | Q |
| A. | W、X、Y中最简单氢化物稳定性最弱的是Y | |
| B. | Q元素形成的单质微粒间作用力除了分子间作用力还含有共价键 | |
| C. | M元素氧化物对应水化物的酸性一定强于Z | |
| D. | 电解饱和的NaM溶液可以制取H2和NaMX |
15.关于如图各装置的叙述正确的是( )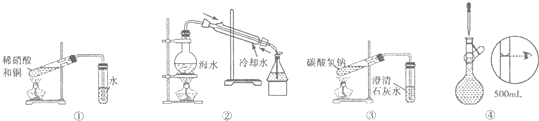

| A. | 装置①可用于实验室制备NO气体 | |
| B. | 装置②可用于模拟海水蒸馏 | |
| C. | 装置③可用于探究碳酸氢钠的热稳定性 | |
| D. | 装置④为配制溶液过程中的定容操作 |
12.下列各项操作中,能发生“先沉淀后溶解”现象的是( )
①向BaCl2溶液中通入过量的SO2
②向Fe(OH)3胶体中逐滴滴入过量稀H2SO4
③向Na[Al(OH)4]溶液中逐滴加入过量的AlCl3溶液
④向澄清石灰水中通入过量的SO2
⑤向硅酸钠溶液中通入过量的CO2
⑥向AgNO3溶液中逐滴加入过量的氨水.
①向BaCl2溶液中通入过量的SO2
②向Fe(OH)3胶体中逐滴滴入过量稀H2SO4
③向Na[Al(OH)4]溶液中逐滴加入过量的AlCl3溶液
④向澄清石灰水中通入过量的SO2
⑤向硅酸钠溶液中通入过量的CO2
⑥向AgNO3溶液中逐滴加入过量的氨水.
| A. | ②④⑥ | B. | ①②④ | C. | ①③⑤⑥ | D. | ②③④⑤ |
19.SO2是无色有窒息性臭味的有毒气体,是一种主要的气态污染物.某化学兴趣小组制备并对SO2的化学性质和用途进行探究.
 【SO2的制备】
【SO2的制备】
(1)用亚硫酸钠与浓硫酸反应制备SO2的装置如图1(夹持仪器省略).图1中的装置错误的是C(填字母);D的作用是吸收二氧化硫尾气,防止污染空气.
【探究SO2的性质】
(2)根据SO2中S元素的化合价,预测并通过实验验证SO2的性质.实验可选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、FeCl3溶液、品红溶液等.探究过程实验装置如图2.(夹持仪器省略)
①请完成表格.
②A中发生反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++4H++SO42-.
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案二:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.上述方案不合理的是方案一,原因是过量的二氧化硫能溶于水,也能使高锰酸钾褪色.
【SO2的用途】
(3)二氧化硫通常作为保护剂添加到葡萄酒中,有杀菌、抗氧化、改善风味和增酸的作用,但吸吸入过量二氧化硫对人体有害.我国国家标准规定葡萄酒中SO2的最大使用量为0.25g•L-1.图3为该小组对葡萄酒中的SO2进行收集与测量的装置.
①冷凝管中水的进口为:a(填“a”或“b”)
②A中加入200.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为SO2+H2O2=H2SO4.
③除去B中过量的H2O2,然后用0.0600mol•L-1NaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液20.00mL,该葡萄酒中SO2含量为:0.192g•L-1.
 【SO2的制备】
【SO2的制备】(1)用亚硫酸钠与浓硫酸反应制备SO2的装置如图1(夹持仪器省略).图1中的装置错误的是C(填字母);D的作用是吸收二氧化硫尾气,防止污染空气.
【探究SO2的性质】
(2)根据SO2中S元素的化合价,预测并通过实验验证SO2的性质.实验可选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、FeCl3溶液、品红溶液等.探究过程实验装置如图2.(夹持仪器省略)
①请完成表格.
| 药品 | 作用 | |
| A | FeCl3溶液 | 验证SO2的还原性 |
| B | Na2S溶液 | 验证二氧化硫的氧化性 |
| C | 品红溶液 | 验证二氧化硫的漂白性 |
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案二:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.上述方案不合理的是方案一,原因是过量的二氧化硫能溶于水,也能使高锰酸钾褪色.
【SO2的用途】
(3)二氧化硫通常作为保护剂添加到葡萄酒中,有杀菌、抗氧化、改善风味和增酸的作用,但吸吸入过量二氧化硫对人体有害.我国国家标准规定葡萄酒中SO2的最大使用量为0.25g•L-1.图3为该小组对葡萄酒中的SO2进行收集与测量的装置.
①冷凝管中水的进口为:a(填“a”或“b”)
②A中加入200.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为SO2+H2O2=H2SO4.
③除去B中过量的H2O2,然后用0.0600mol•L-1NaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液20.00mL,该葡萄酒中SO2含量为:0.192g•L-1.
9.下列有关氧元素及其化合物的表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧原子的结构示意图: | |
| C. | 水分子的电子式: | |
| D. | 乙酸甲酯的结构简式HCOOC2H5 |
16. 分枝酸在微生物、植物的“芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图.下列关于分枝酸的叙述不正确的是( )
分枝酸在微生物、植物的“芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图.下列关于分枝酸的叙述不正确的是( )
 分枝酸在微生物、植物的“芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图.下列关于分枝酸的叙述不正确的是( )
分枝酸在微生物、植物的“芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图.下列关于分枝酸的叙述不正确的是( )| A. | 分枝酸的分子式为C10H10O6 | |
| B. | 1mol分枝酸最多消耗3molNaOH | |
| C. | 分枝酸分子中含2个手性碳原子 | |
| D. | 一定条件下,分枝酸可发生取代、加成、氧化和聚合反应 |
13.处理污水的絮凝剂聚合硫酸铁的化学式是[Fe2(OH)n(SO4)(3-$\frac{n}{2}$)]m,下列有关该物质说法不合理的是( )
| A. | 铁元素的化合价为+3价 | |
| B. | n 取值范围是:0<n≤6 | |
| C. | 不能在酸性较强的环境中使用 | |
| D. | 若n=2时,构成该物质的三种微粒个数比为1:1:1 |
14.用铂电极电解1mol•L-1硫酸铜溶液,当Cu2+浓度下降至原浓度的一半时,停止通电.若要使硫酸铜溶液恢复至原浓度和原体积,溶液中可加入适量的( )
| A. | 硫酸铜 | B. | 硝酸铜 | C. | 氢氧化铜 | D. | 氧化铜粉末 |