题目内容
短周期的五种元素A、B、C、D、E,原子序数依次增大.A、B、C三种元素电子层数之和是5.A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物;E单质用于净化水质.请回答:
(1)写出D在元素周期表中的位置 ,E的原子结构示意图是 .
下列可以验证C与D两元素原子得电子能力强弱的实验事实是 (填写编号).
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,该化合物的空间构型是 .
(3)某些无机物均由A、B、C、D四种元素组成,都既可以与盐酸反应又可以与NaOH溶液反应,写出其中任意一种物质的化学式 ,实验室检验该物质中阳离子的方法是 .
(4)C的一种氢化物与D单质的摩尔质量相等,则该氢化物的电子式为 ;C的另一种氢化物与D的一种氢化物的电子总数相等,实验室制取C的该气态氢化物的化学方程式为 .
(5)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该过程的总离子方程式 .②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为 .
(1)写出D在元素周期表中的位置
下列可以验证C与D两元素原子得电子能力强弱的实验事实是
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,该化合物的空间构型是
(3)某些无机物均由A、B、C、D四种元素组成,都既可以与盐酸反应又可以与NaOH溶液反应,写出其中任意一种物质的化学式
(4)C的一种氢化物与D单质的摩尔质量相等,则该氢化物的电子式为
(5)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该过程的总离子方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:短周期元素A、B、C、D、E原子序数依次增大,B元素原子最外电子层上的电子数是它的电子层数的2倍,则B为碳元素或硫元素,因为B后面有C、D、E三种元素都是短周期元素,所以B为C元素;
A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物,则A为H元素,D为O元素;
由于C元素原子序数介于B、D之间,所以C为N元素,E单质用于净化水质,则E为氯Cl元素,据此进行答题.
A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物,则A为H元素,D为O元素;
由于C元素原子序数介于B、D之间,所以C为N元素,E单质用于净化水质,则E为氯Cl元素,据此进行答题.
解答:
解:短周期元素A、B、C、D、E原子序数依次增大,B元素原子最外电子层上的电子数是它的电子层数的2倍,则B为碳元素或硫元素,因为B后面有C、D、E三种元素都是短周期元素,所以B为C元素;A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物,则A为H元素,D为O元素;由于C元素原子序数介于B、D之间,所以C为N元素,E单质用于净化水质,则E为氯Cl元素,
(1)D为O元素,在元素周期表中位于第二周期VIA族;E为Cl元素,氯原子的核电荷数为17,最外层含有7个电子,氯原子结构示意图为: ;
;
A.氢化物的沸点与非金属性强弱没有必然关系,所以无法通过比较这两种元素的气态氢化物的沸点判断非金属性强弱,故A错误;
B.D为O元素、C为D元素,比较只有这两种元素所形成的化合物中的化合价,显示负价的说明其非金属性较强,故B正确;
C.非金属性越强,对应的气态氢化物越稳定,可以通过比较这两种元素的气态氢化物的稳定性判断其非金属性强弱,故C正确;
D.非金属性越强,与氢气形成气态氢化物越容易,可以通过比较这两种元素的单质与氢气化合的难易判断其非金属性强弱,故D正确;
故答案为:第二周期VIA族; ;BCD;
;BCD;
(2)由A、B两种元素组成的最简单的化合物为甲烷,其立体构型是正四面体型,
故答案为:正四面体型;
(3)由A、B、C、D四种元素组成的无机盐甲,既能与盐酸反应又可以与NaOH溶液反应,其化学式为 NH4HCO3或(NH4)2 CO3;该物质中含有铵根离子,检验铵根离子的方法为:取样,加入氢氧化钠溶液并加热,如果生成能使湿润红色石蕊试纸变蓝的气体,则证明铵根离子的存在,
故答案为:NH4HCO3或(NH4)2CO3;取样,加入氢氧化钠溶液并加热,如果生成能使湿润红色石蕊试纸变蓝的气体,则证明铵根离子的存在;
(4)C为N元素、D为O元素,C的一种氢化物与D单质氧气的摩尔质量相等,则C的氢化物的化学式为:N2H4,属于共价化合物,其电子式为: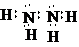 ;
;
C的另一种氢化物与D的一种氢化物的电子总数相等,该C的氢化物为氨气,实验室用氢氧化钙与氯化铵反应制取氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,
故答案为: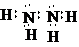 ;2NH4Cl+Ca(OH)2
;2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(5)①CA3为氨气,NH3的水溶液显碱性,可以将Fe2+、Fe3+转化成Fe(OH)2和Fe(OH)3沉淀,在等物质的量的FeSO4和Fe2(SO4)3组成的混合溶液中,反应总离子方程式为:Fe2++2Fe3++8NH3+8H2O═Fe(OH)2↓+2Fe(OH)3↓+8NH4+,
故答案为:Fe2++2Fe3++8NH3+8H2O═Fe(OH)2↓+2Fe(OH)3↓+8NH4+;
②上述反应生成的两种碱继续作用,得到Fe3O4,即氢氧化亚铁与氢氧化铁反应生成四氧化三铁,该反应的化学方程式为:Fe(OH)2+2Fe(OH)3=4H2O+Fe3O4,
故答案为:Fe(OH)2+2Fe(OH)3=4H2O+Fe3O4.
(1)D为O元素,在元素周期表中位于第二周期VIA族;E为Cl元素,氯原子的核电荷数为17,最外层含有7个电子,氯原子结构示意图为:
 ;
;A.氢化物的沸点与非金属性强弱没有必然关系,所以无法通过比较这两种元素的气态氢化物的沸点判断非金属性强弱,故A错误;
B.D为O元素、C为D元素,比较只有这两种元素所形成的化合物中的化合价,显示负价的说明其非金属性较强,故B正确;
C.非金属性越强,对应的气态氢化物越稳定,可以通过比较这两种元素的气态氢化物的稳定性判断其非金属性强弱,故C正确;
D.非金属性越强,与氢气形成气态氢化物越容易,可以通过比较这两种元素的单质与氢气化合的难易判断其非金属性强弱,故D正确;
故答案为:第二周期VIA族;
 ;BCD;
;BCD;(2)由A、B两种元素组成的最简单的化合物为甲烷,其立体构型是正四面体型,
故答案为:正四面体型;
(3)由A、B、C、D四种元素组成的无机盐甲,既能与盐酸反应又可以与NaOH溶液反应,其化学式为 NH4HCO3或(NH4)2 CO3;该物质中含有铵根离子,检验铵根离子的方法为:取样,加入氢氧化钠溶液并加热,如果生成能使湿润红色石蕊试纸变蓝的气体,则证明铵根离子的存在,
故答案为:NH4HCO3或(NH4)2CO3;取样,加入氢氧化钠溶液并加热,如果生成能使湿润红色石蕊试纸变蓝的气体,则证明铵根离子的存在;
(4)C为N元素、D为O元素,C的一种氢化物与D单质氧气的摩尔质量相等,则C的氢化物的化学式为:N2H4,属于共价化合物,其电子式为:
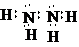 ;
;C的另一种氢化物与D的一种氢化物的电子总数相等,该C的氢化物为氨气,实验室用氢氧化钙与氯化铵反应制取氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2
| ||
故答案为:
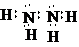 ;2NH4Cl+Ca(OH)2
;2NH4Cl+Ca(OH)2
| ||
(5)①CA3为氨气,NH3的水溶液显碱性,可以将Fe2+、Fe3+转化成Fe(OH)2和Fe(OH)3沉淀,在等物质的量的FeSO4和Fe2(SO4)3组成的混合溶液中,反应总离子方程式为:Fe2++2Fe3++8NH3+8H2O═Fe(OH)2↓+2Fe(OH)3↓+8NH4+,
故答案为:Fe2++2Fe3++8NH3+8H2O═Fe(OH)2↓+2Fe(OH)3↓+8NH4+;
②上述反应生成的两种碱继续作用,得到Fe3O4,即氢氧化亚铁与氢氧化铁反应生成四氧化三铁,该反应的化学方程式为:Fe(OH)2+2Fe(OH)3=4H2O+Fe3O4,
故答案为:Fe(OH)2+2Fe(OH)3=4H2O+Fe3O4.
点评:本题考查位置、结构与性质关系的应用,题目难度中等,推断元素名称为解题关键,试题知识点较多、综合性较强,注意基础知识的理解掌握,明确原子结构与元素周期表、元素周期律之间的关系.

练习册系列答案
相关题目
在一条件下,反应N2+3H2?2NH3在10L恒容密闭容器中进行,测得3min内,N2的物质的量由25mol减少到10mol,则3min内N2的化学反应速率为( )
| A、1.2mol?L-1?min-1 |
| B、1.0 mol?L-1?min-1 |
| C、0.5 mol?L-1?min-1 |
| D、0.4 mol?L-1?min-1 |
化学与生产、生活、社会密切相关.下列有关说法中,不正确的是( )
| A、PM2.5的颗粒物,分散在空气中可形成胶体 |
| B、汽车尾气不仅能形成光化学污染还能破坏臭氧层 |
| C、对废旧电池进行回收处理主要为了防止重金属污染水源 |
| D、富含氮、磷的生活污水不能排放到河中,但可以直接用于农田的灌溉 |
