题目内容
7.反应A+3B=2C+2D在不同条件下反应速率如下,其中最快的是反应( )| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) | |
| C. | v(C)=0.4mol/(L•min) | D. | v(D)=0.0075 mol/(L•s) |
| A. | A | B. | B | C. | C | D. | D |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质的速率与其化学计量数的比值越大,表示反应速率越快,注意单位保持一致.
解答 解:A.$\frac{v(A)}{1}$=0.15mol/(L•min),
B.$\frac{v(B)}{3}$=0.2mol/(L•min);
C.$\frac{v(C)}{2}$=0.2mol/(L•min)
D.v(D)=0.0075 mol/(L•s)=v(D)=0.45 mol/(L•min),$\frac{v(D)}{2}$=0.225mol/(L•min),
故反应速率v(D)>v(B)=v(C)>v(A),
故选:D.
点评 本题考查化学反应速率快慢比较,难度不大,利用比值法可以迅速判断,也可以转化为同一物质的速率进行比较.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列说法正确的是( )
| A. | 含金属元素的离子不一定是阳离子 | |
| B. | 金属单质跟酸反应,一定放出氢气 | |
| C. | 元素从化合态变为游离态时,一定被氧化 | |
| D. | 元素从化合态变为游离态时,一定被还原 |
18.下列结论正确的是( )
①离子还原性:S2->I->Fe2+>Br-
②氢化物沸点HF<HCl<HBr
③酸性:H2SO4>HClO4
④非金属性:F>Cl>S.
①离子还原性:S2->I->Fe2+>Br-
②氢化物沸点HF<HCl<HBr
③酸性:H2SO4>HClO4
④非金属性:F>Cl>S.
| A. | ②④ | B. | ①④ | C. | ①②③ | D. | 只有④ |
15.ZnC2、Al4C3、Mg2C3、Li2C2等与CaC2和H2O反应相似.下列说法不正确的是( )
| A. | C22-的电子式是[ ]2- ]2- | |
| B. | Mg2C3和Li2C2与水反应生成的烃可能具有相同的官能团 | |
| C. | 1mol ZnC2与水反应生成的烃的体积约为22.4L | |
| D. | Al4C3与水反应生成的烃分子中只有极性键 |
2.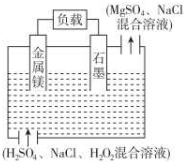 镁-过氧化氢电池是一种新型的高性能电源,其结构如图所示,下列说法不正确的是( )
镁-过氧化氢电池是一种新型的高性能电源,其结构如图所示,下列说法不正确的是( )
 镁-过氧化氢电池是一种新型的高性能电源,其结构如图所示,下列说法不正确的是( )
镁-过氧化氢电池是一种新型的高性能电源,其结构如图所示,下列说法不正确的是( )| A. | 镁作该电源负极,发生反应Mg-2e-═Mg2+ | |
| B. | 该电池反应方程式:Mg+H2O2+2H+═Mg2++2H2O | |
| C. | 放电时溶液中的Cl-向正极移动 | |
| D. | 放电时正极周围溶液的pH升高 |
16.下列Cl2既表现氧化性又表现还原性的反应是( )
| A. | Cl2+2NaOH═NaCl+NaClO+H2O | B. | Cl2+H2O═HCl+HClO | ||
| C. | Cl2+Cu$\frac{\underline{\;点燃\;}}{\;}$CuCl2 | D. | Cl2+H2$\frac{\underline{\;点燃\;}}{\;}$2HCl |

