题目内容
13.下列化学用语表达错误的是( )| A. | NH3的电子式: | B. | Al2O3+3H2 $\stackrel{高温}{→}$ 2Al+3H2O | ||
| C. | 氯离子的结构示意图: | D. | N原子的轨道表示式: |
分析 A.氨气为共价化合物,分子中含有3个N-H,N原子最外层满足8电子稳定结构;
B.铝的活泼性较强,无法用氢气还原,通常采用电解法制取金属铝;
C.氯离子的核电荷数为17,核外电子总数为18,最外层满足8电子稳定结构;
D.N原子核外电子总数为5,结合构造原理判断其核外电子轨道表示式.
解答 解:A.氨气分子中含有3个N-H'键,NH3的电子式为 ,故A正确;
,故A正确;
B.由于Al的活泼性较强,用氢气无法置换出铝,该反应不会发生,故B错误;
C.氯离子的核电荷数为17,最外层满足8电子稳定结构,其离子的结构示意图为: ,故C正确;
,故C正确;
D.N原子的核外电子总数为5,其轨道表示式为: ,故D正确;
,故D正确;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及离子结构示意图、化学方程式、电子轨道表示式、电子式等知识,明确常见化学用语的书写原则为解答关键,试题有利于提高学生的规范答题能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
3.下列有机反应中,有一种反应类型与其他3种反应类型不同的是( )
| A. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| D. | 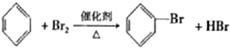 |
1.在下列条件下,两种气体的分子数一定相等的是( )
| A. | 同温度,同体积的N2和O2 | B. | 同质量,不同密度的N2和CO | ||
| C. | 同压强,同体积的H2和CH4? | D. | 同体积,同密度的CO2和N2 |
8.碳酸有两个电离常数Ki1、Ki2,分别对应碳酸的两步电离.关于Ki1和Ki2说法正确的是( )
| A. | Ki1的表达式为Ki1=$\frac{[{H}_{2}C{O}_{3}]}{[{H}^{+}][HC{{O}_{3}}^{-}]}$ | |
| B. | Ki2对应的电离过程是HCO3-+H2O?H3O++CO32- | |
| C. | 当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 | |
| D. | 改变条件使Ki1减小,则Ki2一定也减小 |
18.下列微粒在溶液中能大量共存的是( )
| A. | NH4+、Mg2+、SO42-、CH3COO- | B. | HCO3-、K+、Cl-、AlO2- | ||
| C. | Cu2+、Na+、SO42-、HS- | D. | Na+、H+、SO42-、S2O32- |
5.下列实验目的可以达到的是( )
| A. | 将滴有稀硫酸的淀粉溶液加热后,加入新制的Cu(OH)2悬浊液,加热,没有红色沉淀,说明淀粉在该条件下没有水解 | |
| B. | 将铜与足量的浓硝酸反应生成的气体干燥后收集,用冰水混合物冷却降温,研究温度对化学平衡的影响 | |
| C. | 将混合气体通过饱和Na2CO3溶液以便除去CO2中少量的SO2 | |
| D. | 某无色溶液中加入Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
2.下列有机物的结构简式和名称都正确的是( )
| A. | 2-甲基丁醛 CH3CH2 (CH3)CHCOH | B. | 硬酯酸甘油脂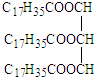 | ||
| C. | TNT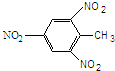 | D. | α-氨基丙酸 CH3CH(NH2)COOH |
3.下列物质的水溶液因水解呈酸性的是( )
| A. | FeCl3 | B. | Na2CO3 | C. | CH3COOH | D. | KHSO4 |