题目内容
下列关于反应Zn+2HNO3+NH4NO3═N2↑+3H2O+Zn(NO3)2的说法中正确的是( )
| A、N2只是还原产物,Zn(NO3)2只是氧化产物 |
| B、NH4NO3只是氧化剂,Zn是还原剂 |
| C、反应中生成1 mol N2时共有5 mol电子发生转移 |
| D、HNO3在反应中没有表现出酸性 |
考点:氧化还原反应,硝酸的化学性质
专题:氧化还原反应专题
分析:Zn+2HNO3+NH4NO3═N2↑+3H2O+Zn(NO3)2中,Zn元素的化合价升高,N元素的化合价由-3价升高为0,N元素的化合价由+5价降低为0,以此来解答.
解答:
解:Zn+2HNO3+NH4NO3═N2↑+3H2O+Zn(NO3)2中,Zn元素的化合价升高,N元素的化合价由-3价升高为0,N元素的化合价由+5价降低为0,
A.N2是还原产物也是氧化产物,Zn(NO3)2只是氧化产物,故A错误;
B.NH4NO3是还原剂,Zn是还原剂,故B错误;
C.由硝酸中N元素的化合价变化可知,反应中生成1 molN2时共有5mol电子发生转移,故C正确;
D.HNO3在反应中生成硝酸锌,表现出酸性,故D错误;
故选C.
A.N2是还原产物也是氧化产物,Zn(NO3)2只是氧化产物,故A错误;
B.NH4NO3是还原剂,Zn是还原剂,故B错误;
C.由硝酸中N元素的化合价变化可知,反应中生成1 molN2时共有5mol电子发生转移,故C正确;
D.HNO3在反应中生成硝酸锌,表现出酸性,故D错误;
故选C.
点评:本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,侧重氧化还原反应中的基本概念、转移电子数的考查,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列关于胶体的叙述错误的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 |
| B、光线透过胶体时,胶体中可发生丁达尔效应 |
| C、可用过滤的方法分离FeCl3溶液和Fe(OH)3胶体 |
| D、Fe(OH)3胶体能吸附水中悬浮的固体颗粒,而使之沉降,达到净水目的 |
下列变化需加入氧化剂才能完成的是( )
| A、MnO4-→MnO2 |
| B、HCO3-→CO2 |
| C、S2-→HS- |
| D、Br-→Br2 |
下列用离子方程式的书写中,正确的是( )
| A、用石英与烧碱溶液反应制备防火剂硅酸钠溶液:SiO2+2OH-=SiO32-+H2O |
| B、用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、用氯化铁溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ |
| D、用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2↑ |
 [化学--选修5有机化学基础]
[化学--选修5有机化学基础]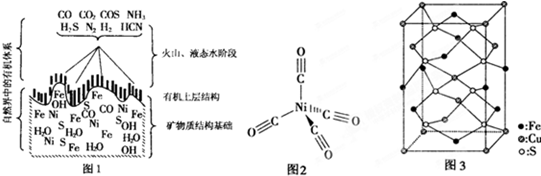
 化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.