题目内容
13.将Cl2通入自来水中杀菌消毒,主要是利用了Cl2和H2O生成的HClO的( )| A. | 强氧化性 | B. | 酸性 | C. | 还原性 | D. | 稳定性 |
分析 氯气与水反应生成HCl和HClO,HClO具有强氧化性,可用于杀菌消毒.
解答 解:氯气和水反应生成盐酸和次氯酸,次氯酸有强氧化性,病菌属于蛋白质,强氧化性物质易使蛋白质变性而杀菌消毒,故选A.
点评 本题考查HClO的性质和应用,在元素化合物知识中经常考查,难度不大.

练习册系列答案
相关题目
3.考古学常用14C来确定文物的历史年代,14C原子核内中子数是( )
| A. | 6 | B. | 8 | C. | 14 | D. | 20 |
1.下列实验方案不可行的是( )
| A. | 用碱石灰干燥氨气 | |
| B. | 用紫色石蕊试液检验酸性溶液 | |
| C. | 通入Cl2除去FeCl3溶液中的FeCl2 | |
| D. | 加入Fe粉除去Al3+溶液中的杂质Cu2+ |
8.下列化合物中,不能由单质直接化合而得到的是( )
| A. | SiO2 | B. | HCl | C. | FeCl2 | D. | NO |
18.已知x、y、z元素的原子具有相同的电子层数,最高价氧化物对应水化物酸性依次增强,则下列判断正确的是( )
| A. | 原子半径按x、y、z顺序增大 | B. | 阴离子的还原性按x、y、z顺序增强 | ||
| C. | 单质的氧化性按x、y、z顺序增强 | D. | 氢化物的稳定性按x、y、z顺序减弱 |
5.下列关于元素周期律的说法正确的是( )
| A. | 酸性强弱:H3PO4<H2SO4 | B. | 稳定性:HF>H2S | ||
| C. | 碱性:Ca(OH)2<Mg(OH)2 | D. | 非金属性:N<Si |
3.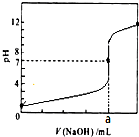 常温下,用0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LHCl溶液,滴定曲线,如图所示.下列说法不正确的是( )
常温下,用0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LHCl溶液,滴定曲线,如图所示.下列说法不正确的是( )
 常温下,用0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LHCl溶液,滴定曲线,如图所示.下列说法不正确的是( )
常温下,用0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LHCl溶液,滴定曲线,如图所示.下列说法不正确的是( )| A. | a=20.00 | |
| B. | 滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-) | |
| C. | 若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 | |
| D. | 若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a<20.00 |
4.将一定量的氯气通入氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3的共存体系.下列判断不正确的是( )
| A. | 参加反应所需NaOH与氯气的物质的量之比一定为2:1 | |
| B. | 反应体系中n(NaCl):n(NaClO):n(NaC1O3)(物质的量之比)可能为11:1:2 | |
| C. | 若反应有amol氯气参加反应,则amol<转移电子数<$\frac{5a}{3}$mol | |
| D. | 反应中NaC1O和NaClO3为氧化产物,且物质的量之比一定为l:1 |
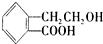 ,它可通过不同的化学反应分别制得B、C和D(下图)三种物质.
,它可通过不同的化学反应分别制得B、C和D(下图)三种物质.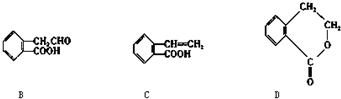
 ;
;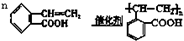 ;
;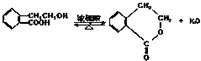 .
.