题目内容
在相同条件下完全燃烧甲烷、丙烷、乙烯,如生成相同质量的水,则甲烷、丙烷、乙烯的体积比是( )
| A、1:1:1 |
| B、1:2:1 |
| C、2:1:1 |
| D、2:1:2 |
考点:有关混合物反应的计算
专题:有机物分子组成通式的应用规律
分析:甲烷、丙烷、乙烯燃烧生成相同质量的水,则甲烷、丙烷、乙烯中H原子的物质的量相同,以此来解答.
解答:
解:甲烷、丙烷、乙烯燃烧生成相同质量的水,则甲烷、丙烷、乙烯中H原子的物质的量相同,
设H原子的物质的量均为8mol,则CH4、C3H8、C2H4的物质的量分别为2mol、1mol、2mol,
相同条件下,甲烷、丙烷、乙烯的体积比是2mol:1mol:2mol=2:1:2,
故选D.
设H原子的物质的量均为8mol,则CH4、C3H8、C2H4的物质的量分别为2mol、1mol、2mol,
相同条件下,甲烷、丙烷、乙烯的体积比是2mol:1mol:2mol=2:1:2,
故选D.
点评:本题考查有机物燃烧有关计算,难度不大,侧重分析能力、计算能力的考查,注意根据H原子守恒进行解答.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
实验室常用饱和的NaNO2与NH4Cl溶液反应制取少量的氮气.反应的化学方程式如下:NaNO2+NH4Cl
NaCl+N2↑+2H2O,则氮气的发生装置与下列气体中发生装置相同的是( )
| ||
| A、H2 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
我国劳动人民在3000多年前就制造出精美的青铜器,青铜是铜锡合金,具有良好的可铸造性.耐磨性和耐腐蚀性.取青铜样品8.1g,经分析其中含锡0.9g,此青铜中铜与锡的质量比是( )
| A、9:2 | B、9:1 |
| C、8:1 | D、4:1 |
分析如下残缺的反应:RO3-+ +6H+=3R2↑+3H2O.下列叙述正确的是( )
| A、上式中缺项所填物质在反应中作氧化剂 | ||
| B、R的原子半径在同周期元素原子中最小 | ||
| C、R一定是周期表中的第VA族元素 | ||
D、RO
|
有关纯碱和小苏打的叙述正确的是( )
| A、等质量的Na2CO3、NaHCO3分别与足量的稀盐酸反应,NaHCO3产生的CO2多 |
| B、等质量的Na2CO3、NaHCO3分别与足量的同浓度盐酸反应,NaHCO3消耗的盐酸多 |
| C、向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| D、Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠溶液反应 |
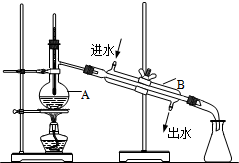 如图为实验室制取自来水的装置示意图,根据图示回答下列问题.
如图为实验室制取自来水的装置示意图,根据图示回答下列问题.