题目内容
7. 如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )
如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )| A. | X代表的元素处于第ⅥA族 | |
| B. | Y的最低负化合价是-3 | |
| C. | M元素的最高价氧化物对应的水化物的化学式是HMO3 | |
| D. | 气态氢化物的稳定性:N>Z |
分析 如图是元素周期表的一部分,表格中所示元素均为前四周期的元素,可知X为第二周期,Y、M为第三周期,Z、N为第四周期,X元素的非金属性在同周期中仅次于一种元素,则X为O元素,结合元素在周期表中的位置可知Y为P元素、M为Cl元素,Z为Se元素,N为Br元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:由以上分析可知X为O元素、Y为P元素、Z为Se元素、M为C元素、N为Br元素.
A.由以上分析可知X为O元素,处于第ⅥA族,故A正确;
B.Y为P元素,最低负化合价是-3,故B正确;
C.M为C元素,最高化合价为+4价,最高价氧化物对应的水化物的化学式是H2MO3,故C错误;
D.同周期元素从左到右非金属性增强,元素的非金属性越强,对应的氢化物越稳定,则气态氢化物的稳定性:N>Z,故D正确.
故选C.
点评 本题考查结构性质位置关系应用,为高频考点,推断元素是解题关键,侧重对元素周期律的考查,注意对基础知识的理解掌握.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
7.下列叙述正确的是( )
| A. | NaHCO3溶液中:c(H+)+c(Na+)═c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)一样多 | |
| C. | 0.2mol•L-1 HCl溶液与等体积0.05 mol•L-1 Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 向10 mL 0.10mol•L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
2.二氯化碳利用具有十分重要的意义,科学家有以下几个设想.
(1)用太阳能将CO2转化成O2和C(石墨烯),其设想如图1:
①Fe3O4中Fe的化合价是+2和+3;
②重整系统发生反应的化学方程式为6FeO+CO2═2Fe3O4+C.
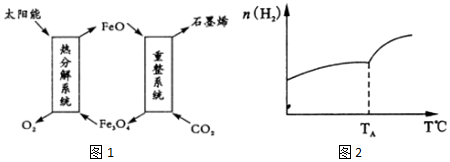
(2)二氧化碳和氢气在催化剂作用下可制取低碳烯烃.在一密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g)?C2H4 (g)+4H2O(g)△H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图2所示.
①其它条件不变,起始时若按lmolCO2、2molH2进行投料,CO2转化率将减小(填“增大”、“减小”或“不变”);
②△H<0(填“>”“<”“不能确定”).
③若测试中体系内无氧气产生,试结合图示推断热稳定性C2H4<H2O (填“>”“<”“不能确定”).
(3)用氨水吸收CO2制化肥(NH4HCO3)
①已知:NH3•H2O(aq)?NH4+(aq)+OH-(aq)△H1=a kJ•mol-1
CO2 (g)+H2O(l)?H2CO3 (aq)△H2=bkJ•mol-1
H2CO3(aq)+OH-(aq)?HCO3-(aq)+H2O(l)△H3=ckJ•mol-1
则利用NH3•H2O吸收CO2制备NH4HCO3的热化学方程式为NH3•H2O+CO2═NH4++HCO3-△H=(a+b+c)kJ/mol;
②已知常温下相关数据如表:
则反应NH4++HCO3-+H2O?NH3•H2O+H2CO3的平衡常数k=1.25×10-3.
(1)用太阳能将CO2转化成O2和C(石墨烯),其设想如图1:
①Fe3O4中Fe的化合价是+2和+3;
②重整系统发生反应的化学方程式为6FeO+CO2═2Fe3O4+C.

(2)二氧化碳和氢气在催化剂作用下可制取低碳烯烃.在一密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g)?C2H4 (g)+4H2O(g)△H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图2所示.
①其它条件不变,起始时若按lmolCO2、2molH2进行投料,CO2转化率将减小(填“增大”、“减小”或“不变”);
②△H<0(填“>”“<”“不能确定”).
③若测试中体系内无氧气产生,试结合图示推断热稳定性C2H4<H2O (填“>”“<”“不能确定”).
(3)用氨水吸收CO2制化肥(NH4HCO3)
①已知:NH3•H2O(aq)?NH4+(aq)+OH-(aq)△H1=a kJ•mol-1
CO2 (g)+H2O(l)?H2CO3 (aq)△H2=bkJ•mol-1
H2CO3(aq)+OH-(aq)?HCO3-(aq)+H2O(l)△H3=ckJ•mol-1
则利用NH3•H2O吸收CO2制备NH4HCO3的热化学方程式为NH3•H2O+CO2═NH4++HCO3-△H=(a+b+c)kJ/mol;
②已知常温下相关数据如表:
| Kb(NH3•H2O) | 2×10-5mol•L-1 |
| Ka1(H2CO3) | 4×10-7mol•L-1 |
| Ka2(H2CO3) | 4×10-11mol•L-1 |
19.有关如图所示有机化合物的说法不正确的是( )


| A. | 该有机物的分子式为C15H18O4 | |
| B. | 1 mol该化合物最多可以与2 mol NaOH反应 | |
| C. | 既可以催化加氢,又可以使酸性KMnO4溶液褪色 | |
| D. | 可以与NaHCO3溶液反应放出CO2气体 |
16.化学在自然资源的开发和利用中具有重要的意义,下列对其认识不正确的是( )
| A. | 利用化学知识和化学规律,人们可以更好的开发和利用资源 | |
| B. | 人们在开发和利用资源的过程中,对环境造成了污染,化学对此无能为力 | |
| C. | 利用化学知识和化学规律,人们可以制取更多物质,丰富物质世界 | |
| D. | 人们对资源的开发和利用过程中,时刻不能忘记资源的可持续性发展 |
17.实验室进行粗盐提纯,无需进行的操作是( )
| A. | 分液 | B. | 溶解 | C. | 过滤 | D. | 蒸发 |

 ,名称是环己烷.
,名称是环己烷.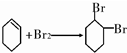 .
.

 ,则①是E,②是D,③是A(填字母),其中装置E的作用是i观察气体的通入速率ⅱ混合氯气和氮气ⅲ除去氯气中的氯化氢
,则①是E,②是D,③是A(填字母),其中装置E的作用是i观察气体的通入速率ⅱ混合氯气和氮气ⅲ除去氯气中的氯化氢