��Ŀ����
4��2016��3��10�գ��п�Ժ�Ϻ������ǿ�����������ص�ʵ���������������ó�ǿ�̼���ɹ����������ʣ������ҹ���ѧ���״����ü���ɹ����������ʣ����ʺͷ������ǶԳƵģ����������ɷ����ӹ��ɣ������ӵ���������������������������ȫ��ͬ����������ɵĵ����෴������÷����Ӻͷ����Ӵ���ԭ�Ӻ��е����Ӻ����ӣ��͵õ���ԭ�Ӻˣ������������ӣ����γɷ�ԭ�ӣ���ԭ�ӹ��ɷ����ӣ��������ɷ����ʣ�����ѡ�������ǣ�������| A�� | ��ԭ�ӵĽṹʾ��ͼΪ�� ������ԭ�ӵĽṹʾ��ͼΪ�� ������ԭ�ӵĽṹʾ��ͼΪ��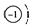 | |
| B�� | ����ԭ������һ��������ɵķ����Ӻ�һ��������ɵķ����� | |
| C�� | ����ԭ�ӵ�Ħ������Ϊ1g/mol | |
| D�� | 21H�ķ���ԭ������2��������ɵķ����� |
���� �������֪����ԭ��ԭ�Ӻ�����һ�����ӣ������磬������һ�����ӣ������磬�ɱ�ʾΪ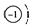 ���Դ˽����⣮
���Դ˽����⣮
��� �⣺A����ԭ�Ӻͷ���ԭ�ӵ����ӡ����ӵ���෴����A��ȷ��
B���������Ϣ��֪������ԭ������һ��������ɵķ����Ӻ�һ��������ɵķ����ӣ���B��ȷ��
C���������䣬����ԭ�ӵ�Ħ������Ϊ1g/mol����C��ȷ��
D��21H�ķ���ԭ������������Ϊ1����1��������ɵķ����ӣ���D����
��ѡD��
���� ������������Ϣ�⣬Ϊ��Ƶ���㣬�����ڿ���ѧ���ķ�����������ѧ�������ѶȲ���ע�����ԭ�ӵĹ��ɣ���ѧ��Ӧ����������Դ��֪ʶ��

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
15������˵����ȷ���ǣ�������
| A�� | �������ʵ�����ʾ���ӡ�ԭ�ӡ����ӡ�����������С�������� | |
| B�� | Ħ���ǹ��ʵ�λ���е��߸�����������֮һ | |
| C�� | 1mol�κ����ʶ����� 6.02��1023��ԭ�� | |
| D�� | 0.012Kg12C����̼ԭ����Ϊ6.02��1023 |
12�������ǻ�ѧѧϰ���о��ij����ֶΣ����з������ݺͽ��۶���ȷ���ǣ�������
| A�� | ���Ȼ�̼-�ǵ���� �Ȼ���-ǿ����� ̼��-������� | |
| B�� | NO2-���������� CuO-���������� Al2O3-���������� | |
| C�� | �����ᡢ���â������ʯ�ҷֱ������ᡢ��Ρ������� | |
| D�� | ��ơ�������Һ��ˮ�������ײ��Ͼ�Ϊ���� |
19������2mol•L-1 K2SO4��Һ������˵����ȷ���ǣ�������
| A�� | ��Һ�к���2mol K2SO4 | B�� | �ɽ�2mol K2SO4����1Lˮ���Ƶ� | ||
| C�� | ��Һ��c��K+ ��=4 mol•L-1 | D�� | 1L ��Һ�к�4molK+��4molSO42- |
9������˵����ȷ���ǣ�������
| A�� | ������ԭ��Ӧһ�������Ĵ������Ӧ���� | |
| B�� | ������ԭ��Ӧ�У���Ӧ�ﲻ�����������ǻ�ԭ�� | |
| C�� | ��������ԭ��Ӧ�У��������ͻ�ԭ���ȿ����Dz�ͬ����Ҳ������ͬ������ | |
| D�� | ʧ����Խ�࣬��ԭ��Խǿ���õ���Խ�࣬������Խǿ |
1����������������Ӧ����1molˮ�����ų�241.8kJ��������1molˮ����ת��ΪҺ̬ˮ�ų�4.5kJ���������������Ȼ�ѧ����ʽ��д��ȷ���ǣ�������
| A�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-285.9kJ/mol | B�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-241.8kJ/mol | ||
| C�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=+285.9kJ/mol | D�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=+241.8kJ/mol |