题目内容
14.下列有机反应的产物中不可能存在同分异构体的是( )| A. | CH3CH═CH2与HCl加成 | |
| B. | CH3CH2CH2Cl在碱性溶液中水解 | |
| C. | CH2═CH-CH═CH2与H2按物质的量之比为1﹕1进行反应 | |
| D. | 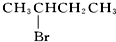 与NaOH的醇溶液共热 与NaOH的醇溶液共热 |
分析 根据同分异构体是分子式相同,但结构不同的化合物.
A、CH3-CH=CH2不是对称结构,与氯化氢发生加成反应,氯原子可以连接在中间碳原子上,也可以连接在不饱和的端碳原子上;
B、CH3CH2CH2Cl与NaOH水溶液共热发生取代反应,-OH取代Br原子,生成CH3CH2CH2OH;
C、CH2=CH-CH=CH2与H2按物质的量之比1:1加成,可能发生1,2-加成,也可能出1,4-加成;
D、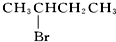 不是对称结构,与溴原子相连碳相邻碳原子上有2种化学环境不同的氢原子,发生消去反应有2种产物.
不是对称结构,与溴原子相连碳相邻碳原子上有2种化学环境不同的氢原子,发生消去反应有2种产物.
解答 解:A、CH3-CH=CH2一定条件下与HCl加成,可以生成1-氯丙烷,也可以生成2-氯丙烷,存在同分异构体,故A不符合;
B、CH3CH2CH2Br与NaOH水溶液共热发生取代反应,-OH取代Br原子,生成CH3CH2CH2OH,不存在同分异构体,故B符合;
C、CH2=CH-CH=CH2与H2按物质的量之比1:1加成,生成1-丁烯或1,3-丁二烯,存在同分异构体,故C不符合;
D、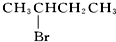 在氢氧化钠醇溶液存在下,发生分子内脱水,生成1-丁烯或2-丁烯,存在同分异构体,故D不符合.
在氢氧化钠醇溶液存在下,发生分子内脱水,生成1-丁烯或2-丁烯,存在同分异构体,故D不符合.
故选B.
点评 本题以加成反应与消去反应为载体,考查同分异构体、常见有机物的性质等,掌握加成反应与消去反应的反应原理是解题的原理.

练习册系列答案
相关题目
2.下列物质中羟基氢原子的活动性由强到弱的顺序正确的是( )
①水 ②乙醇 ③苯酚 ④碳酸.
①水 ②乙醇 ③苯酚 ④碳酸.
| A. | ①②③④ | B. | ①③②④ | C. | ④③②① | D. | ④③①② |
9.下列反应在钢铁的生锈过程中没有发生的是( )
| A. | O2+2H2O+4e-=4OH- | B. | Fe-3e-=Fe3+ | ||
| C. | Fe-2e-=Fe2+ | D. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
19.下列微粒中,与甲烷分子具有相同的质子数和相同的电子数的是( )
| A. | H2O | B. | HCl | C. | NH4+ | D. | OH- |
6.两串联电解池,左边放硫酸铜,右边放一定量的某硝酸盐溶液,电解时当左池有1.6g Cu析出时,右池析出5.4g固体,则右池溶质为( )
| A. | AgNO3 | B. | NaNO3 | C. | Mg(NO3)2 | D. | Al(NO3)3 |
13.表为元素周期表的一部分,其中的编号代表所对应的元素.请回答下列问题:

(1)⑧号元素的基态原子的价电子排布式是3d84s2,与其同周期,且基态原子的核外未成对电子数最多的元素是Cr (写出元素符号).
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是MgO>CaO.
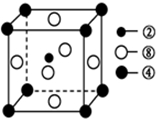
(3)①号与③号元素形成的含有18电子的分子为过氧化氢(写出名称),该分子中③号元素的原子的杂化方式为sp3.②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为MgNi3C(用对应的元素符号表示).
(4)下表是某些短周期元素的电负性值:
①通过分析电负性值变化规律,确定N最接近的电负性值范围:2.5<N<3.5.
②推测电负性值与原子半径关系是半径越大,电负性值越小.
③试推断:AlBr3中化学键类型是共价键.

(1)⑧号元素的基态原子的价电子排布式是3d84s2,与其同周期,且基态原子的核外未成对电子数最多的元素是Cr (写出元素符号).
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是MgO>CaO.
(3)①号与③号元素形成的含有18电子的分子为过氧化氢(写出名称),该分子中③号元素的原子的杂化方式为sp3.②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为MgNi3C(用对应的元素符号表示).

(4)下表是某些短周期元素的电负性值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.1 |
②推测电负性值与原子半径关系是半径越大,电负性值越小.
③试推断:AlBr3中化学键类型是共价键.
 合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.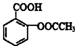 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为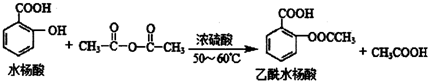
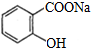 .
.