题目内容
8.下列条件下,两瓶气体所含原子数一相等的是( )| A. | 同质量的N2和CO2 | B. | 同质量的H2和N2 | ||
| C. | 同体积的O2和N2 | D. | 相同物质的量的N2O和CO2 |
分析 A、根据n=$\frac{m}{M}$计算;
B、二者同质量,摩尔质量不相同,则物质的量不同;
C、二者体积相同,物质的量不一定相等;
D、二者分子物质的量相同,分子数相同,都是双原子分子,原子数目相同.
解答 解:A、n=$\frac{m}{M}$可知原子的物质的量分别为:$\frac{m}{28}$×2、$\frac{m}{44}$×3,所以含原子数不相同,故A错误;
B、同质量的H2和N2,二者同质量,摩尔质量不相同,则物质的量不同,两种分子都含有2个原子,所以原子数不相同,故B错误;
C、二者体积相同,由于压强和温度不一定相同,所以物质的量不一定相等,则含原子数不一定相同,故C错误;
D、相同物质的量的N2O和CO2,也就是分子数相同,这两种分子还都含有2个原子,所以原子数相同,故D正确.
故选:D.
点评 本题考查了阿伏伽德罗定律及推论,难度不大,注意公式的灵活运用,可借助pV=nRT理解.

练习册系列答案
相关题目
18. 2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )
2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )
 2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )
2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )| A. | 分子式为C15H22O5 | B. | 属于芳香族化合物 | ||
| C. | 可发生水解反应 | D. | 含有过氧键(-O-O-)有强氧化性 |
19.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 常温下,23g NO2和N2O4的混合气体含有NA个氧原子 | |
| B. | 1L0.1mol•L-1的氨水含有0.1NA个OH- | |
| C. | 标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA | |
| D. | 1molFe与1molCl2充分反应,转移3NA个电子 |
16.下列实验设计方案或判断中正确的是( )
| A. | 加入足量铜粉后,搅拌、可过滤可除去Cu(NO3)2溶液中混有的AgNO3 | |
| B. | 通过装有NaOH溶液的确洗气瓶来除去CO2中混有的HCl气体 | |
| C. | 某无色未知溶液中加入BaCl2溶液,有白色沉淀,可推断溶液中的一定含有SO42- | |
| D. | 未知溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则溶液中一定大量含CO32- |
3.下列说法正确的是( )
| A. | 制氧气时,用Na2O2或H2O2作反应物应该选择不同的气体发生装置 | |
| B. | 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| C. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀时的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
17.下列叙述中,正确的是( )
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℃/30MPa}^{催化剂}$2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| D. | 含 1mol NaOH的稀溶液分别和含1mol CH3COOH、1mol HNO3的稀溶液反应,后者比前者放出的热量多 |
18.将0.4mol/L的NH4Cl溶液与0.2mol/L的NaOH溶液等体积混合,则混合溶液中下列离子的浓度关系正确的是( )
| A. | c ( NH4+)+c ( Na+)=c ( Cl-)+c ( OH-) | |
| B. | c ( NH4+)+c ( NH3•H2O )=0.4mol/L | |
| C. | c ( Cl-)>c ( NH4+)>c ( Na+)>c ( OH-)>c ( H+) | |
| D. | c ( Cl-)>c ( Na+)>c ( NH4+)>c ( H+ )>c ( OH-) |
 ;B的结构简式是
;B的结构简式是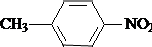 .
.