题目内容
18. 2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )
2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键-线结构简式如图.下列关于青蒿素的说法不正确的是( )| A. | 分子式为C15H22O5 | B. | 属于芳香族化合物 | ||
| C. | 可发生水解反应 | D. | 含有过氧键(-O-O-)有强氧化性 |
分析 由结构简式可知分子式,含-COOC-、醚键及过氧键,结合酯、过氧化物的性质来解答.
解答 解:A.由结构简式可知有机物分子式为C15H22O5,故A正确;
B.有机物不含苯环,不是芳香族化合物,故B错误;
C.含有酯基,可发生水解反应,故C正确;
D.含有过氧键,具有强氧化性,故D正确.
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查基本概念、物质结构等知识点,明确官能团及其性质关系是解本题关键,易错选项是A.

练习册系列答案
相关题目
14.某碳氢化合物分子的结构式如图: ,下列有关该分子的叙述正确的是( )
,下列有关该分子的叙述正确的是( )
 ,下列有关该分子的叙述正确的是( )
,下列有关该分子的叙述正确的是( )| A. | 该分子含5个σ键,3个π键 | |
| B. | 该分子是非极性分子 | |
| C. | 该分子的碳原子均是以sp2杂化轨道参与成键 | |
| D. | 分子中有4个原子在同一直线上 |
15.亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危 害.其在酸性条件下会产生NO和NO2.下列有关说法错误的是( )
| A. | NaNO2既具有氧化性又具有还原性 | |
| B. | 1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol | |
| C. | NaNO2和胃酸作用的离子方程式为:2NO${\;}_{2}^{-}$+2H+=NO↑+NO2↑+H2O | |
| D. | 食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害 |
6.下列各组物质按熔点由低到高的顺序排列的是( )
| A. | O2、S、Br2 | B. | CH4、SiH4、GeH4 | C. | Li、Na、K | D. | H2O、H2S、H2Se |
13.下列叙述正确的是( )
| A. | 在标准状况下1mol任何物质所占体积都是22.4升 | |
| B. | 当压强大于101KPa时1mol任何气体的体积都小于22.4升 | |
| C. | 在相同条件下,两种物质的量相同的气体必然具有相同的原子数 | |
| D. | 气体摩尔体积的数值受温度和压强的影响 |
3.下列离子能大量共存,且满足相应条件的是( )
| 选项 | 离子组 | 条件 |
| A | K+、Na+、Cu2+、Cl- | 溶液呈无色 |
| B | Na+、Fe3+、NO3-、SO42- | 滴入酸性KMnO4溶液,溶液褪色 |
| C | Al3+、SO42-、Cl-、H+ | 加入氨水产生白色沉淀后沉淀溶解 |
| D | Na+、NO3-、I-、SO42- | 加入盐酸和淀粉溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |
7.下表是元素周期表的一部分,针对表中的 种元素回答下列有关问题:
(1)在这些元素中,最活泼金属元素的原子结构示意图为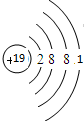 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式 ,
,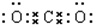 .
.
(4)用电子式表示元素④与⑥构成化合物的形成过程: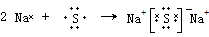 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.
(5)能说明④与⑧金属性强弱的事实是分别与冷水反应,K与水的反应现象更剧烈,则钠比钾金属性的弱(举一例)
(6)设计实验方案比较⑥与⑦非金属性强弱
Cl2、S分别与H2反应
硫化钠和氯气反应.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ |
 ,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).
,最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式表示).(2)②、③、⑤、⑥、⑦形成的气态氢化物中最稳定的是HF(填化学式).
(3)④与②组成的某种化合物和①与②组成的某种化合物反应生成氧气,写出这两种化合物的电子式
 ,
,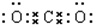 .
.(4)用电子式表示元素④与⑥构成化合物的形成过程:
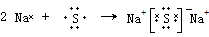 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.(5)能说明④与⑧金属性强弱的事实是分别与冷水反应,K与水的反应现象更剧烈,则钠比钾金属性的弱(举一例)
(6)设计实验方案比较⑥与⑦非金属性强弱
Cl2、S分别与H2反应
硫化钠和氯气反应.
8.下列条件下,两瓶气体所含原子数一相等的是( )
| A. | 同质量的N2和CO2 | B. | 同质量的H2和N2 | ||
| C. | 同体积的O2和N2 | D. | 相同物质的量的N2O和CO2 |
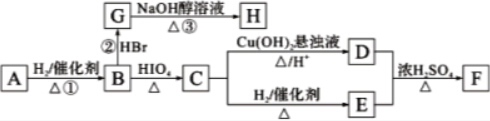
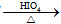 RCHO+R′CHO
RCHO+R′CHO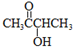 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为
.若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为 .
. .
.