题目内容
7.依据图1中氮元素及其化合物的转化关系,回答问题: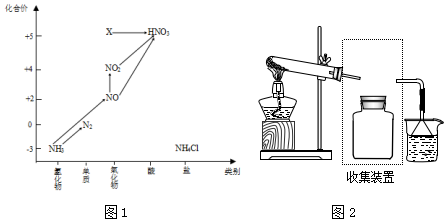
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2H2O+2NH3↑.
(2)若要收集一瓶氨气,请将下列装置补充完整,在图2虚框内画出连接图.
(3)下列试剂不能用于干燥NH3的是A.
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$ 4NO+6H2O.
②NO→NO2实验现象是无色气体变为红棕色.
③NO2H2O→HNO3氧化剂与还原剂物质的量之比为1:2.
(5)图1中,实验室只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为H2O2 .
(6)图1中,X的化学式为N2O5,从物质性质上看,X属于酸性氧化物.将X转化为HNO3属于非氧化还原反应(填“氧化还原”或“非氧化还原”).
(7)若要将NH3→N2,从原理上看,下列试剂可行的是AD.
A.O2B.NaC.NH4ClD.NO2.
分析 (1)实验室常用NH4Cl与Ca(OH)2制取氨气,生成氯化钙、氨气和水;
(2)氨气极易溶于水,比空气轻,收集方法只能用向下排空气法收集,导气管位置短进长出;
(3)氨气是碱性气体,干燥气体选用碱性干燥剂;
(4)①氨气催化氧化生成一氧化氮和水;
②一氧化氮和氧气反应生成二氧化氮;
③二氧化氮和水反应生成硝酸和一氧化氮;
(5)只用一种物质将NO直接转化为硝酸且绿色环保,无尾气排放;
(6)图1分析可知XX化合价与硝酸相同为+5价,物质类型为氧化物;
(7)若要将NH3→N2,氮元素化合价-3价变化为0价,氨气做还原剂被氧化;
解答 解:(1)实验室常用NH4Cl与Ca(OH)2制取氨气,生成氯化钙、氨气和水,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2H2O+2NH3↑,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2H2O+2NH3↑;
(2)氨气极易溶于水,比空气轻,收集方法只能用向下排空气法收集,导气管位置短进长出,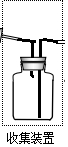 ,
,
故答案为: ;
;
(3)A.浓硫酸和氨气反应,不能干燥氨气,故A错误;
B.碱石灰是氢氧化钠和氧化钙固体,可以干燥氨气,故B正确;
C.NaOH固体吸收水分不与氨气反应,可以干燥氨气,故C正确
故答案为:A;
(4)①NH3→NO反应是氨气的催化氧化,反应的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$ 4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$ 4NO+6H2O;
②NO→NO2实验现象是无色气体变化为红棕色气体,
故答案为:无色气体变为红棕色;
③二氧化氮和水反应生成一氧化氮和硝酸,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应中二氧化氮化合价+4价变化为+5价和+2价,氧化剂与还原剂物质的量之比为1;,2,
故答案为:1:2;
(5)图1中,实验室只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为H2O2,3H2O2+2NO=2HNO3+2H2O,
故答案为:H2O2 ;
(6)图1分析可知XX化合价与硝酸相同为+5价,物质类型为氧化物,X化学式为:N2O5,N2O5为酸性氧化物,N2O5+H2O=2HNO3,反应为非氧化还原反应,
故答案为:N2O5;酸性;非氧化还原;
(7)(7)若要将NH3→N2,氮元素化合价-3价变化为0价,氨气做还原剂被氧化,A.O2可以氧化氨气为氮气,故A正确;
B.Na是还原剂不能氧化氨气,故B错误;
C.NH4C中氮元素化合价-3价,不能和氨气反应生成氮气,故C错误;
D.NO2和氨气反应做氧化剂,氮元素化合价可以变化为0价,生成氮气,故D正确;
故答案为:A D;
点评 本题考查了氮的化合物及其性质、气体制备、氧化还原反应的理解应用,掌握基础是解题关键,题目难度中等.

| A. | 纯净物 | B. | 溶液 | C. | 胶体 | D. | 浊液 |
| A. | 甘油 | B. | 植物油 | C. | 乙酸乙酯 | D. | 高级脂肪酸 |
| A. | 18 g H2O在标准状况下的体积是22.4 L | |
| B. | 1molFe与足量Cl2完全反应,转移电子2mol | |
| C. | 在常温常压下,22.4 L Cl2含6.02×1023个氯气分子 | |
| D. | 48g O2和O3的混合气体含有3mol氧原子 |
| A. | 氨气遇浓盐酸产生白烟:NH3+HCl═NH4Cl | |
| B. | 打磨过的铝片与NaOH溶液反应产生气体:2Al+2OH-═2AlO2-+H2↑ | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | Fe(OH)2由白色变灰绿,最后变为红褐色:4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| A. | N2 | B. | CO | C. | NO2 | D. | NH3 |
| A. | NaCl、KCl | B. | Na2CO3、KCl | C. | CaCl2、NaCl | D. | K2CO3、CaCl2 |
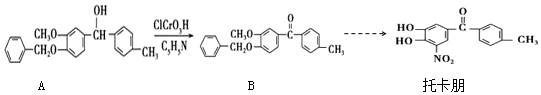
下列说法不正确的是( )
| A. | 托卡朋的分子式为C14H11NO5 | |
| B. | 反应A→B的类型属于取代反应 | |
| C. | 托卡朋分子中所有的碳原子有可能在同平面内 | |
| D. | 托卡朋能发生加成反应 |
| A. | Ag++Cl-→AgCl↓ | B. | Ag++Br-→AgBr↓ | ||
| C. | Ag++CO32-→AgCO3↓ | D. | Ag2CO3+2H+→2Ag++CO2↑+H2O |