题目内容
2.下列解释过程或事实的方程式不正确的是( )| A. | 氨气遇浓盐酸产生白烟:NH3+HCl═NH4Cl | |
| B. | 打磨过的铝片与NaOH溶液反应产生气体:2Al+2OH-═2AlO2-+H2↑ | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | Fe(OH)2由白色变灰绿,最后变为红褐色:4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
分析 A.氨气与氯化氢反应生成氯化铵;
B.2molAl完全反应生成3mol氢气,该反应不满足电子守恒;
C.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水;
D.氢氧化亚铁不稳定,易被空气中氧气氧化成氢氧化铁.
解答 解:A.氨气遇浓盐酸产生白烟,反应的化学方程式为:NH3+HCl═NH4Cl,故A正确;
B.打磨过的铝片与NaOH溶液反应产生气体,正确的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C.NaOH溶液不能保存在玻璃塞的试剂瓶中,原因是二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,反应的离子方程式为:SiO2+2OH-═SiO32-+H2O,故C正确;
D.氢氧化亚铁易被氧化,则Fe(OH)2由白色变灰绿,最后变为红褐色,发生反应的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故D正确;
故选B.
点评 本题考查了离子方程式、化学方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等;试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
12.下列反应的离子方程式书写正确的是( )
| A. | Cl2溶于水:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 盐酸与氢氧化钠溶液反应:H++OH-═H2O | |
| C. | 三氯化铁腐蚀印刷线路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 盐酸与碳酸钙反应制备二氧化碳:CO32-+2H+═CO2↑+H2O |
13.向试管b分别滴加入a中物质,下列对b中现象的解释错误的是( )
| 实验 | a中物质 | b中现象 | 结论或解释 | |
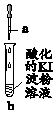 | A. | Fe(OH)3悬浊液 | Fe(OH)3悬浊液溶解,溶液变蓝 | 发生反应:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2 |
| B. | NaClO3溶液 | 先变蓝后褪色 | 褪色的反应:2ClO3-+10I-+12H+═Cl2+5I2+6H2O | |
| C. | \ | 空气中放置一段时间,溶液变蓝 | 发生反应:4I-+4H++O2=2I2+2H2O | |
| D. | 含碘元素的无色溶液 | 溶液呈蓝色 | 可能发生的反应:5I-+IO3-+6H+=3I2+3H2O |
| A. | A | B. | B | C. | C | D. | D |
10.下列仪器中,不能加热的是( )
| A. | 烧瓶 | B. | 烧杯 | C. | 容量瓶 | D. | 蒸发皿 |
17.将一小块金属钠放在坩埚里加热,实验现象描述正确的是( )
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色
③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色
⑤钠燃烧后生成物为淡黄色固体.
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色
③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色
⑤钠燃烧后生成物为淡黄色固体.
| A. | ①④⑤ | B. | 只有⑤ | C. | 只有① | D. | ②③ |
14.当光束通过下列分散系时,可观察到丁达尔效应的是( )
| A. | 硫酸铜溶液 | B. | 氢氧化铁胶体 | C. | 蔗糖溶液 | D. | 氯化钠溶液 |
11.下列有关化学用语表示正确的是( )
| A. | 氨气分子的电子式: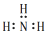 | B. | Mg2+结构示意图  | ||
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U互为同位素 | D. | 乙醇的分子式C2H5OH |