题目内容
某些化学反应可用下式表示:A+B─→C+D+H2O 请回答下列问题:
(1)若A、C、D均含氯元素,且A的化合价介于C与D之间,该反应的离子方程式: .
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,则A与B的组合是: .
(3)若A为黑色固体,C是黄绿色的单质气体,写出该反应的离子方程式:
(4)若A为红色金属单质,B为第二周期某种元素的最高价氧化物的水化物,请写出一个符合上式的化学方程式: .
(5)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 .
(1)若A、C、D均含氯元素,且A的化合价介于C与D之间,该反应的离子方程式:
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,则A与B的组合是:
(3)若A为黑色固体,C是黄绿色的单质气体,写出该反应的离子方程式:
(4)若A为红色金属单质,B为第二周期某种元素的最高价氧化物的水化物,请写出一个符合上式的化学方程式:
(5)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是
考点:无机物的推断
专题:推断题
分析:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应;
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,碳酸氢钠或碳酸钠都能和盐酸反应生成氯化钠、二氧化碳和水;
(3)若A为黑色固体,C是黄绿色的单质气体,则A为二氧化锰,B为浓盐酸,C为氯气,二氧化锰与浓盐酸反应制氯气;
(4)若A为红色金属,应为Cu,B为第二周期某种元素的最高价氧化物的水化物,则B是硝酸,铜和浓硝酸(或稀硝酸)反应生成硝酸铜、二氧化氮(或一氧化氮)和水;
(5)若C、D均为气体且都能使澄清石灰水变浑浊,应为SO2和CO2,在加热条件下,浓硫酸和碳发生氧化还原反应生成二氧化碳和二氧化硫.
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,碳酸氢钠或碳酸钠都能和盐酸反应生成氯化钠、二氧化碳和水;
(3)若A为黑色固体,C是黄绿色的单质气体,则A为二氧化锰,B为浓盐酸,C为氯气,二氧化锰与浓盐酸反应制氯气;
(4)若A为红色金属,应为Cu,B为第二周期某种元素的最高价氧化物的水化物,则B是硝酸,铜和浓硝酸(或稀硝酸)反应生成硝酸铜、二氧化氮(或一氧化氮)和水;
(5)若C、D均为气体且都能使澄清石灰水变浑浊,应为SO2和CO2,在加热条件下,浓硫酸和碳发生氧化还原反应生成二氧化碳和二氧化硫.
解答:
解:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应,反应的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,碳酸氢钠或碳酸钠都能和盐酸反应生成氯化钠、二氧化碳和水,所以A和B的组合NaHCO3和盐酸或Na2CO3和盐酸,
故答案为:NaHCO3和盐酸或Na2CO3和盐酸;
(3)若A为黑色固体,C是黄绿色的单质气体,则A为二氧化锰,B为浓盐酸,C为氯气,二氧化锰与浓盐酸反应制氯气,反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O,
Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(4)若A为红色金属,应为Cu,B为第二周期某种元素的最高价氧化物的水化物,则B是硝酸,铜和浓硝酸(或稀硝酸)反应生成硝酸铜、二氧化氮(或一氧化氮)和水,化学反应方程式为Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,或3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,
故答案为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,或3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;
(5)若C、D均为气体且都能使澄清石灰水变浑浊,应为SO2和CO2,在加热条件下,浓硫酸和碳发生氧化还原反应生成二氧化碳和二氧化硫,
故答案为:碳和浓硫酸.
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,碳酸氢钠或碳酸钠都能和盐酸反应生成氯化钠、二氧化碳和水,所以A和B的组合NaHCO3和盐酸或Na2CO3和盐酸,
故答案为:NaHCO3和盐酸或Na2CO3和盐酸;
(3)若A为黑色固体,C是黄绿色的单质气体,则A为二氧化锰,B为浓盐酸,C为氯气,二氧化锰与浓盐酸反应制氯气,反应的离子方程式为MnO2+4H++2Cl-
 Mn2++Cl2↑+2H2O,
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
 Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;(4)若A为红色金属,应为Cu,B为第二周期某种元素的最高价氧化物的水化物,则B是硝酸,铜和浓硝酸(或稀硝酸)反应生成硝酸铜、二氧化氮(或一氧化氮)和水,化学反应方程式为Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,或3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,
故答案为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,或3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;
(5)若C、D均为气体且都能使澄清石灰水变浑浊,应为SO2和CO2,在加热条件下,浓硫酸和碳发生氧化还原反应生成二氧化碳和二氧化硫,
故答案为:碳和浓硫酸.
点评:本题考查了无机物的推断,同时考查学生掌握知识的全面性及分析问题、解决问题的能力,明确物质的性质是解本题关键,结合物质之间的转化来分析解答,注意二氧化硫和二氧化碳都能使澄清石灰水变浑浊,为易错点.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
目前海水提溴的最主要方法之一是空气吹出法工艺,其流程图如下:以下推断不合理的是( )


| A、热空气能吹出溴是利用溴易挥发的性质 |
| B、SO2吸收溴的反应方程式:SO2+2H2O+Br2→H2SO4+2HBr |
| C、流程中循环利用的物质有SO2、Br2、Cl2等多种 |
| D、没有采用直接蒸馏含溴海水得到单质溴的主要原因是为了节能 |
下列实验操作不正确的是( )
A、 蒸发食盐水 |
B、 取固体粉末 |
C、 加热液体 |
D、 倾倒液体 |
下列有关说法正确的是( )
A、由-CH3、 、-OH、-COOH四种原子团两两组合形成的有机物中,属于弱电解质的有4种 、-OH、-COOH四种原子团两两组合形成的有机物中,属于弱电解质的有4种 | ||
B、某种兴奋剂的结构简式如图 ,1mol该物质与浓溴水反应时最多消耗Br2为6mol ,1mol该物质与浓溴水反应时最多消耗Br2为6mol | ||
C、有机物X、Y、M的转化关系为:淀粉→X→Y
| ||
D、高分子化合物 ,其链节为对苯二甲酸和乙二醇 ,其链节为对苯二甲酸和乙二醇 |
常温下,0.1mol?L-1的一元酸HA与0.1mol?L-1的NaOH溶液等体积混合后,所得溶液pH>7,下列说法正确的是( )
| A、混合前一元酸HA的c(H+)=0.1 mol?L-1 |
| B、该混合溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C、HA在水溶液中的电离方程式:HA=H++A- |
| D、该混合溶液中:c(A-)+c(HA)=0.1 mol?L-1 |
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、Z的说法正确的是( )


| A、相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B、Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
| C、ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D、由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
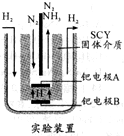 氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.