题目内容
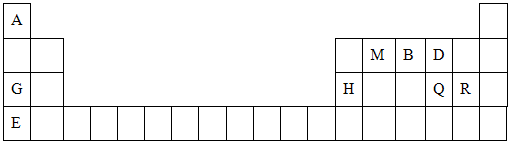
元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。
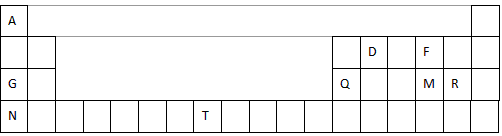
(1)表中T的元素符号为___________ ,金属性最强的元素是_________ (填元素符号)。
(2)元素的非金属性:M_________ R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是__________ 。
(4)F、G两元素形成的淡黄色固体物质的电子式为_______,该物质含有的化学键的类型是________。
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是 ___________(填离子符号)。
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为________ 。
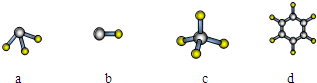
(7)A与D形成分子的空间结构可能是(填序号)________ 。
(2)元素的非金属性:M_________ R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是__________ 。
(4)F、G两元素形成的淡黄色固体物质的电子式为_______,该物质含有的化学键的类型是________。
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是 ___________(填离子符号)。
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为________ 。
(7)A与D形成分子的空间结构可能是(填序号)________ 。
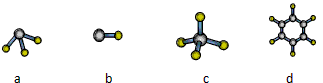
(1)Fe;K。
(2)<
(3)HClO4
(4) ;离子键、非极性共价键
;离子键、非极性共价键
(5)S2->Cl->K+
(6)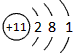
(7)cd
(2)<
(3)HClO4
(4)
 ;离子键、非极性共价键
;离子键、非极性共价键(5)S2->Cl->K+
(6)
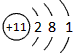
(7)cd

练习册系列答案
相关题目
元素周期表是学习物质结构和性质的重要工具,元素周期律反映了元素性质的周期性变化规律。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有 种不同运动状态的电子,该原子核外共有 种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号) 。
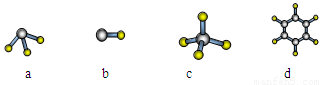
(2)下列变化规律中正确的是 。
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为 ,E的化学式为 。
|
氢化物 |
A |
B |
HF |
D |
E |
|
沸点/℃ |
1317 |
100 |
19.5 |
33 |
164 |