题目内容
20.下列电子式书写正确的是( )| A. | 四氯化碳  | B. | 甲醇  | C. | 羟基  | D. | 甲基 |
分析 A.四氯化碳中,氯原子最外层为 8个电子,漏掉了氯原子的3对电子;
B.O和碳、氢原子相连;
C.羟基是电中性基团;
D.甲基中碳原子有1个单电子未成对.
解答 解:A.四氯化碳为共价化合物,氯原子和碳原子最外层都达到8电子稳定结构,四氯化碳的电子式为: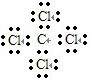 ,故A错误;
,故A错误;
B.甲醇为共价化合物,其结构式为 ,每一个短线代表一对电子,则其电子式为:
,每一个短线代表一对电子,则其电子式为: ,故B错误;
,故B错误;
C.羟基是电中性基团,电子式为 ,故C错误;
,故C错误;
D.甲基中碳原子有1个单电子未成对,甲基电子式为 ,故D正确.
,故D正确.
故选D.
点评 本题考查了电子式的书写判断,题目难度中等,注意掌握电子式的概念及书写方法,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
相关题目
10.下列叙述正确的是( )
| A. | Li在氧气中燃烧主要生成Li2O | |
| B. | 卤族元素单质X2(X:代表F、Cl、Br、I)均可以与水反应生成HX | |
| C. | 将SO2通入次氯酸钙溶液可能得到次氯酸 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
11.下列元素在自然界中以化合态存在的是( )
①Na ②Cl ③Al ④Fe.
①Na ②Cl ③Al ④Fe.
| A. | ① | B. | ①② | C. | ①②③ | D. | ①②③④ |
8.在FeCl3溶液中,加入过量的铜粉,充分反应后,溶液中一定不存在的金属离子是( )
| A. | Fe2+和Cu2+ | B. | Fe3+ | C. | Cu2+ | D. | Fe2+ |
15.研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
请回答下列问题:
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
| 离子 | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
5.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命.二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH.下列有关二甘醇的叙述正确的是( )
| A. | 不能发生消去反应 | B. | 能氧化为酮 | ||
| C. | 能与Na反应 | D. | 不能发生取代反应 |
9.下列实验操作或装置(略去部分夹持仪器)正确的是( )
| A. |  配制溶液 配制溶液 | B. |  碳酸氢钠受热分解 碳酸氢钠受热分解 | ||
| C. |  制备乙酸乙酯 | D. |  制备收集干燥的氨气 |


 .
. .
. ;
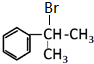
; ,其一氯代物有4种.
,其一氯代物有4种. 依据氧化还原反应:Cu+2Fe3+═Cu2++Fe3+设计的原电池如图.请回答下列问题:
依据氧化还原反应:Cu+2Fe3+═Cu2++Fe3+设计的原电池如图.请回答下列问题: