题目内容
5.已知A、B、C、D均是气体,反应A+B?C+D的能量变化如图所示,下列说法正确的是( )
| A. | 反应物的总键能量低于生成物的总键能 | |
| B. | 该反应是放热反应 | |
| C. | 当A的正反应速率与C的逆反应速率相同时处于平衡状态 | |
| D. | 当A、B、C、D的浓度相同时,反应处于平衡状态 |
分析 A、反应物键能和大于生成物键能和时,反应放热;
B、反应物总能量大于生成物,反应吸热;
C、正逆反应式速率相等时,反应处于平衡状态;
D、A、B、C、D的浓度大小决定于开始加入的反应物多少和反应程度.
解答 解:A、反应物总能量大于生成物,反应吸热,故A错误;
B、该反应吸热,反应物键能和大于生成物,故B错误;
C、A与C的化学计量数相同,所以当A的正反应速率与C的逆反应速率相同时说明正逆反应速率相等,反应处于平衡状态,故C正确;
D、A、B、C、D的浓度大小决定于开始加入的反应物多少和反应程度,与反应是否达到平衡状态无关,故D错误;
故选C.
点评 本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
15.下列事实不能证明醋酸是弱酸的是( )
| A. | 常温下,测得醋酸钠溶液的pH>7 | |
| B. | 醋酸可以使紫色石蕊试液变红 | |
| C. | 物质的量浓度相同时,锌粒跟盐酸反应的速率比与醋酸反应的快 | |
| D. | 常温下,测得0.1 mol/L醋酸溶液的pH>1 |
20.图是元素周期表的一部分,下列说法正确的是( )
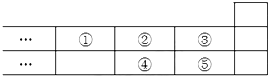

| A. | 元素①位于第二周期第IVA族 | |
| B. | 元素的最高正价是③=⑤ | |
| C. | 最高价氧化物对应水化物的酸性:③>⑤>④ | |
| D. | 气态氢化物的稳定性:④<②<③ |
10.太阳能光伏发电系统是被称为“21世纪绿色光源”的半导体照明(LED)系统(如图).已知发出白光的LED是将GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成.下列说法中不正确的是( )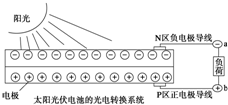

| A. | 光伏发电是将太阳能转变为电能 | |
| B. | Ga与N在元素周期表中不处于同一主族 | |
| C. | YAG中钇显+3价 | |
| D. | 上图中N区半导体为负极,P区半导体为正极,电流从a流向b |
17.铝材经脱脂后进行碱洗以除去氧化膜,将碱洗后的溶液中的铝以沉淀形式回收,最好加入下列试剂( )
| A. | 氨水 | B. | CO2 | C. | NaOH | D. | HNO3 |
7.用石墨电极电解1molL -1的下列溶液,溶液的pH不变的是( )
| A. | HCl | B. | NaOH | C. | Na 2SO 4 | D. | NaCl |
 .
. .
.


