题目内容
20.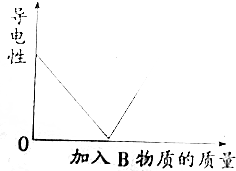 向某A溶液中加入一种物质B,其导电能力变化与加入B物质的质量关系符合如图曲线的是( )
向某A溶液中加入一种物质B,其导电能力变化与加入B物质的质量关系符合如图曲线的是( )| A. | 盐酸中滴加Ba(OH)2溶液至过量 | |
| B. | CaCl2溶液中滴加浓Na2CO3溶液至过量 | |
| C. | AgNO3溶液中滴加NaCl溶液至过量 | |
| D. | 稀硫酸中滴加Ba(OH)2溶液至过量 |
分析 电解质溶液的导电性与离子浓度成正比、与电荷成正比,根据图知,随着B物质的加入,溶液的导电性降低,说明溶液中离子浓度减小,当导电性为0时,溶液中没有溶质,只有水,继续加入B物质,溶液中离子浓度增大,溶液的导电性增大,则在加入B物质过程中,A、B反应生成难溶性固体或生成水或气体,据此分析解答.
解答 解:电解质溶液的导电性与离子浓度成正比、与电荷成正比,根据图知,随着B物质的加入,溶液的导电性降低,说明溶液中离子浓度减小,当导电性为0时,溶液中没有溶质,只有水,继续加入B物质,溶液中离子浓度增大,溶液的导电性增大,则在加入B物质过程中,A、B反应生成难溶性固体和水,
A.盐酸中滴加Ba(OH)2溶液至过量,二者反应方程式为2HCl+Ba(OH)2=BaCl2+2H2O,反应过程中溶液中溶质转化为可溶性氯化钡,离子浓度变化不变,则导电性变化不大,故A不选;
B.CaCl2溶液中滴加浓Na2CO3溶液至过量,二者反应方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl,溶液中溶质转化为可溶性NaCl,离子浓度变化不大,则溶液导电性变化不大,故B不选;
C.AgNO3溶液中滴加NaCl溶液至过量,二者反应方程式为AgNO3+NaCl=AgCl↓+NaNO3,溶液中溶质转化为可溶性NaNO3,离子浓度变化不大,则溶液导电性变化不大,故C不选;
D.稀硫酸中滴加Ba(OH)2溶液至过量,二者反应方程式:H2SO4+Ba(OH)2=BaSO4↓+2H2O,反应过程中离子浓度变化较大,溶液导电性变化较大,当二者恰好反应时溶液不导电,符合图象,故D选;
故选D.
点评 本题考查电解质溶液导电性,侧重考查学生分析判断能力,电解质溶液导电性与离子浓度有关,与电解质强弱无关,为易错题.

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案| A. | 6.02×1023个碳-12原子就是阿伏加德罗常数 | |
| B. | 1mol氧含6.02×1023个O2分子 | |
| C. | 1molCaCl2中含3mol离子 | |
| D. | 0.5molCl2含1mol氯 |
| A. | CO→CO2 | B. | FeCl2 →FeCl3 | C. | Na2SO3 →SO2 | D. | CuO→Cu |

已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致Al(OH)3溶解、Mg(OH)2沉淀.
(3)物质循环使用,能节约资源上述实验中,可以循环使用的物质是CaCO3或CO2.
(4)高温煅烧碱式碳酸镁aMgCO3•bMg(OH)2•cH2O得到MgO.取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO2 0.896L,通过计算确定碱式碳酸镁的化学式为4MgCO3•Mg(OH)2•4H2O.(写出计算过程,否则不得分)
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p1${\;}^{2{2}^{3}}$③1s22s22p2④1s22s22p63s23p4 原子半径最大的是① | |
| B. | 具有下列价电子排布式的原子中,①3s23p1 ②3s23p 2 ③3s23p3 ④33s23p 4第一电离能最大是③ | |
| C. | ①Na、K、Rb ②N、P、Si ③Na、P、Cl,元素的电负性随原子序数增大而递增的是③ | |
| D. | 某主族元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+ |