题目内容
下列说法正确的是( )
| A、Al2O3固体不导电且不溶于水,它在水溶液中不导,所以Al2O3不是电解质 |
| B、Na2SO4溶液导电,所以Na2SO4溶液是电解质 |
| C、CO2的水溶液可以导电,CO2是电解质 |
| D、1.5mol/L的NaCl溶液与1.0mol/L的MgCl2溶液相比较,导电能力后者强 |
考点:电解质与非电解质
专题:
分析:A.在水溶液里或熔融状态下能导电的化合物是电解质;
B.电解质必需是化合物;
C.电解质能自身电离出离子;
D.导电能力和离子浓度和所带电荷有关.
B.电解质必需是化合物;
C.电解质能自身电离出离子;
D.导电能力和离子浓度和所带电荷有关.
解答:
解:A.在水溶液里或熔融状态下能导电的化合物是电解质;Al2O3固体不导电但熔融状态下能导电,所以Al2O3是电解质,故A错误;
B.电解质必需是化合物,Na2SO4溶液是混合物,不是电解质,故B错误;
C.电解质能自身电离出离子,二氧化碳溶于水和水结合成碳酸电离出离子,故二氧化碳为非电解质,故C错误;
D.导电能力和离子浓度和所带电荷有关,1.5mol/L的NaCl溶液与1.0mol/L的MgCl2溶液相比较离子总浓度都为3mol/L,但镁离子所带电荷多,故导电能力强,故D正确;
故选D.
B.电解质必需是化合物,Na2SO4溶液是混合物,不是电解质,故B错误;
C.电解质能自身电离出离子,二氧化碳溶于水和水结合成碳酸电离出离子,故二氧化碳为非电解质,故C错误;
D.导电能力和离子浓度和所带电荷有关,1.5mol/L的NaCl溶液与1.0mol/L的MgCl2溶液相比较离子总浓度都为3mol/L,但镁离子所带电荷多,故导电能力强,故D正确;
故选D.
点评:本题考查了电解质的概念,难度不大,注意电解质首先必须是化合物,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
对于胃溃疡较重的病人,不适合使用的抑酸剂是( )
| A、Mg(OH)2 |
| B、Al(OH)3 |
| C、NaHCO3 |
| D、Na3C6H5O7?2H2O |
下列不属于金属的通性的是( )
| A、导电导热性 | B、延展性 |
| C、有光泽 | D、熔点很高 |
下列有关说法正确的是( )
| A、盐酸可以导电,所以盐酸是电解质 |
| B、氧化还原反应中都只有一种元素化合价升高 |
| C、纳米材料也是一种胶体 |
| D、丁达尔效应,是胶体粒子对光散射形成的 |
下列有关物理量相应的单位表达中,错误的是( )
| A、摩尔质量g/mol |
| B、气体摩尔体积mol/L |
| C、溶解度g |
| D、密度g/cm3 |
某粒子的结构示意图为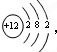 ,关于该粒子的说法不正确的是( )
,关于该粒子的说法不正确的是( )
 ,关于该粒子的说法不正确的是( )
,关于该粒子的说法不正确的是( )| A、属于金属离子 |
| B、核外有三个电子层 |
| C、核电荷数为12 |
| D、在化学反应中溶液失去2个电子 |
在标准状况下,与12克氢气体积相等的氮气的( )
| A、质量为12克 |
| B、物质的量为6摩尔 |
| C、体积为22.4L/mol |
| D、物质的量为12mol |