题目内容
下列有关叙述正确的是( )
| A、液体氯化氢、液氮、液氯都是电解质 |
| B、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、NaCl为离子化合物,HCl为共价化合物,它们的判断方法是看熔融状态是否导电 |
| D、BaSO4的水溶液不易导电,故BaSO4是弱电解质 |
考点:电解质与非电解质
专题:物质的组成专题
分析:A.液氨是非电解质,液氯是单质,它既不是电解质也不是非电解质;
B.电解质是水溶液中或熔融状态下能导电的化合物;
C.离子化合物熔融状态能电离,共价化合物在熔融时不电离;
D.硫酸钡是难溶的盐,熔融状态完全电离.
B.电解质是水溶液中或熔融状态下能导电的化合物;
C.离子化合物熔融状态能电离,共价化合物在熔融时不电离;
D.硫酸钡是难溶的盐,熔融状态完全电离.
解答:
解:A.液氨在水中不能自身电离,是非电解质;液氯是单质,它既不是电解质也不是非电解质;液态氯化氢是电解质,故A错误;
B.电解质是水溶液中或熔融状态下能导电的化合物,SO3溶于水后能导电是因为和水反应生成的H2SO4能电离,和SO3本身无关,是非电解质,故B错误;
C.离子化合物熔融状态能电离,共价化合物在熔融时不电离,所以NaCl为离子化合物,HCl为共价化合物,它们的判断方法是看熔融状态是否导电,故C正确;
D.硫酸钡是难溶的盐,投入水中,导电性较弱,但熔融状态完全电离,所以BaSO4是强电解质,故D错误;
故选:C.
B.电解质是水溶液中或熔融状态下能导电的化合物,SO3溶于水后能导电是因为和水反应生成的H2SO4能电离,和SO3本身无关,是非电解质,故B错误;
C.离子化合物熔融状态能电离,共价化合物在熔融时不电离,所以NaCl为离子化合物,HCl为共价化合物,它们的判断方法是看熔融状态是否导电,故C正确;
D.硫酸钡是难溶的盐,投入水中,导电性较弱,但熔融状态完全电离,所以BaSO4是强电解质,故D错误;
故选:C.
点评:本题主要考查了电解质、非电解质、强电解质、弱电解质的判断等,注意概念间的联系,题目难度不大.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列为制取溴苯实验的有关现象的解释和叙述中正确的是( )
| A、实验室制取的溴苯为褐色的液体,是其中液溴造成的 |
| B、溴苯比水轻,因此溴苯浮在水面上 |
| C、实验室制取溴苯时,导管口出现白雾,是由于HBr遇水蒸气而形成的 |
| D、溴苯和苯的混合物可以用水萃取分离 |
用示意图或图示的方法能够直观形象地将化学知识传播给学生,下列示意图或图示正确的是( )
A、 砷原子结构示意图 |
B、 水合钠离子示意图 |
C、 HF分子间的氢键 |
D、 在通常状况下氢原子电子云示意图 |
“文房四宝”是中华文明的杰出代表,其制作原料或成分分别为:笔(主要是动物毛发)、墨(炭墨烟和动物胶)、纸(植物纤维)、砚(主要成分是硅酸盐).下列说法中不正确的是( )
| A、纸的主要成分属于糖类 |
| B、笔和墨的原料中都存在蛋白质 |
| C、“文房四宝”中只有砚的成分中存在无机物 |
| D、笔、墨、纸、砚中都存在可能发生水解反应的物质 |
将2.7gAl与100ml2mol/LH2SO4溶液充分反应后,再慢慢滴入25ml4mol/LNaOH溶液,其结果是( )
| A、所得溶液的pH为7 |
| B、得到澄清透明的溶液 |
| C、取少量所得溶液,加NaHC03,无明显现象发生 |
| D、另取少量所得溶液,加入几滴NaOH溶液,有白色沉淀 |
下列反应不能一步得到的是( )
| A、Mg→C |
| B、SiO2→H2SiO3 |
| C、Fe→FeCl2 |
| D、Fe3+→Fe2+ |
 可逆反应mA(g)+nB(g)?eC(g)+fD(g),当其它条件不变时,C的百分含量与温度、压强关系如图1,图2所示,下列说法正确的是( )
可逆反应mA(g)+nB(g)?eC(g)+fD(g),当其它条件不变时,C的百分含量与温度、压强关系如图1,图2所示,下列说法正确的是( )| A、达平衡后,使用催化剂C的百分含量变大 |
| B、达平衡后升温,平衡左移 |
| C、方程式系数m+n>e+f |
| D、达平衡后,增加A的量有利于平衡向正反应方向移动 |
13C-NMR(核磁共振)可用于含碳化合物的结构分析,有关13C的说法正确的是( )
| A、质子数为6 |
| B、电子数为13 |
| C、中子数为6 |
| D、质量数为6 |
下列图示关系中不正确的是( )
A、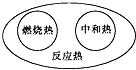 |
B、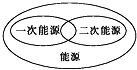 |
C、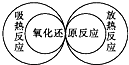 |
D、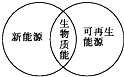 |