题目内容
17.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,2.24L甲烷、戊烷混合物所含分子数为0.1NA | |
| B. | 0.1molC2H6O分子中含有的C-H的数目一定为0.5NA | |
| C. | 1L lmol/L的CH3COONa溶液中所含CH3COO-个数为0.1NA | |
| D. | 标准状况下,2.24L16O2和3.6g18O2含有氧原子均为0.2NA |
分析 A、标况下戊烷为液体;
B、C2H6O分子可能为乙醇,还可能为二甲醚;
C、醋酸根为弱酸根,在溶液中会水解;
D、求出2.24L16O2和3.6g18O2的物质的量,然后根据氧气为双原子分子来分析.
解答 解:A、标况下戊烷为液体,故2.24L甲烷和戊烷的混合物不能根据气体摩尔体积来计算,故A错误;
B、C2H6O分子可能为乙醇,还可能为二甲醚,由于乙醇中含5条C-H键,而二甲醚中含6条C-H键,故0.1mol此分子中含有的C-H键鼠不一定为0.5NA个,故B错误;
C、醋酸根为弱酸根,在溶液中会水解,故溶液中的醋酸根的个数小于0.1NA个,故C错误;
D、标况下2.24L16O2的物质的量为0.1mol,而3.6g18O2的物质的量n=$\frac{3.6g}{36g/mol}$=0.1mol,而氧气均为双原子分子,故0.1mol16O2和18O2中含有的氧原子的个数均为0.2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
7.下列物质中,既含离子键又含有共价键的是( )
| A. | 铁 | B. | 氢氧化钠 | C. | 氯化钠 | D. | 水 |
8.一些常见有机物的转化如图,下列说法正确的是( )


| A. | 上述有机物中只有C6H12O6属于糖类物质 | |
| B. | 物质A和B都属于电解质 | |
| C. | 物质C和油脂类物质互为同系物 | |
| D. | 转化1可在人体内完成,该催化剂属于蛋白质 |
5.下列反应中,生成物的总能量高于反应物的总能量的是( )
| A. | 煅烧石灰石 | B. | 锌与稀硫酸反应 | ||
| C. | NaOH溶液和稀盐酸反应 | D. | 铝热反应 |
12.已知4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
| A. | $\frac{2}{3}$v(NH3)=v(H2O) | B. | 5v(O2)=6v(H2O) | C. | v(NH3):v(O2)=4:5 | D. | $\frac{5}{4}$v(O2)=v(NO) |
2.下列化学用语正确的是( )
| A. | CCl4的电子式: | B. | 中子数为8的碳原子:${\;}_{6}^{14}$C | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | CH4分子的比例模型: |
9.有机物甲、乙的结构如图所示.下列说法错误的是( )


| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能与溴的单质发生加成反应 | |
| C. | 甲、乙都能与金属钠反应生成氢气 | |
| D. | 一定条件下,甲、乙均能发生取代反应 |
15. 有X、Y、Z、W、A、B六种元素.其相关信息如下:
有X、Y、Z、W、A、B六种元素.其相关信息如下:
请回答下列有关问题:
(1)根据信息分析元素Y是F(填元素符号),A在元素周期表中的位置是第四周期VIII.
(2)BX3分子的中心原子采取的杂化类型是sp3.
(3)光谱证实单质 Z与强碱溶液反应生成[Z(OH)4]-,该原子的空间构型是正四面体型,[Z(OH)4]-离子中存在的化学键有ACD (填字母)
A.极性共价键 B.非极性共价键 C.配位键 D.σ键 E.π键
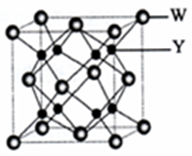
(4)Y与W可形成离子化合物,其晶胞结构如下图所示.W离子采取的堆枳方式是面心立方堆积,W离子的配位数为8,W离子的配位数为此空多余,Y离子占据空位四面体(填“四面体或八面体”).若该晶体的密度为dg•cm-3,则该晶胞中最近的Y离子与W离子间的距离是$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{{N}_{A}×d}}$cm,(设NA为阿佛加德罗常数的值,只需列出计算表达式)
 有X、Y、Z、W、A、B六种元素.其相关信息如下:
有X、Y、Z、W、A、B六种元素.其相关信息如下:请回答下列有关问题:
| 元素 | 相关信息 | ||||||||||||||
| X | X原子的1s轨道上只有1个电子 | ||||||||||||||
| Y | Y是周期表中电负性最大的元素 | ||||||||||||||
| Z | Z是第三周期主族元素,其电离能l1~l7如下表所示(单位:KJ/mol)
| ||||||||||||||
| W | W是主族元素且与A同周期,其最外电子层上有两个运动状态不同的电子 | ||||||||||||||
| A | A是过渡元素,其基态原子的外围电子排布图为: | ||||||||||||||
| B | B元素基态原子的2p轨道中有三个未成对的电子 |
(2)BX3分子的中心原子采取的杂化类型是sp3.
(3)光谱证实单质 Z与强碱溶液反应生成[Z(OH)4]-,该原子的空间构型是正四面体型,[Z(OH)4]-离子中存在的化学键有ACD (填字母)
A.极性共价键 B.非极性共价键 C.配位键 D.σ键 E.π键
(4)Y与W可形成离子化合物,其晶胞结构如下图所示.W离子采取的堆枳方式是面心立方堆积,W离子的配位数为8,W离子的配位数为此空多余,Y离子占据空位四面体(填“四面体或八面体”).若该晶体的密度为dg•cm-3,则该晶胞中最近的Y离子与W离子间的距离是$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{{N}_{A}×d}}$cm,(设NA为阿佛加德罗常数的值,只需列出计算表达式)
16.下列有关实验操作的叙述和与实验得出的相应结论都正确的是( )
| 实验操作 | 结论 | |
| A | 乙醇、浓硫酸混合加热170℃,导出的物质能使酸性高锰酸钾褪色 | 该反应生成了乙烯 |
| B | 在溴乙烷中加入适量的氢氧化钠溶液,加热一段时间,再滴入几滴硝酸银,会有沉淀析出 | 溴乙烷在碱性条件下能水解出Br- |
| C | 提纯粗苯甲酸用重结晶法,主要步骤为:加热溶解、趁热过滤、冷却结晶、过滤、洗涤 | 苯甲酸在水中的溶解度受温度影响很大 |
| D | 可用裂化汽油萃取溴水中的溴,且将有机层从分液漏斗上口倒出 | 裂化汽油密度比水小 |
| A. | A | B. | B | C. | C | D. | D |