题目内容
常温下,以下试剂不能用来鉴别SO2和H2S的是( )
| A、滴有淀粉的碘水 |
| B、氢氧化钠溶液 |
| C、硫酸铜溶液 |
| D、品红溶液 |
考点:物质的检验和鉴别的实验方案设计
专题:
分析:二氧化硫具有还原性可与碘反应,且二氧化硫具有漂白性;硫化氢具有还原性可与碘反应,二氧化硫与硫酸铜可发生复分解反应,二者均与NaOH反应生成盐和水,以此来解答.
解答:
解:A.能使蓝色褪去得到无色溶液的为SO2,生成淡黄色沉淀的为H2S,现象不同,可鉴别,故A不选;
B.二者均与NaOH溶液反应,得到无色溶液,现象相同,不能鉴别,故B选;
C.与硫酸铜混合无变化的为SO2,混合生成黑色沉淀的为H2S,现象不同,可鉴别,故C不选;
D.能使品红褪色的为SO2,无现象的为H2S,现象不同,可鉴别,故D不选;
故选B.
B.二者均与NaOH溶液反应,得到无色溶液,现象相同,不能鉴别,故B选;
C.与硫酸铜混合无变化的为SO2,混合生成黑色沉淀的为H2S,现象不同,可鉴别,故C不选;
D.能使品红褪色的为SO2,无现象的为H2S,现象不同,可鉴别,故D不选;
故选B.
点评:本题考查物质的鉴别,为高频考点,把握物质的性质、发生的反应和反应现象为解答的关键,侧重分析与应用能力的考查,注意现象相同不能鉴别物质,题目难度不大.

练习册系列答案
相关题目
常温下,下列离子在指定条件下能大量共存的是( )
| A、c(I-)=0.1 mol/L的溶液中:Ca2+、NO3-、Fe3+、Cl- |
| B、SO2饱和溶液中:NH4+、K+、CO32-、ClO- |
| C、放入镁带有气体逸出的溶液中:Na+、K+、Cl-、SO42- |
| D、水电离出c(H+)=1×10-10mol/L溶液中:Cu2+、Na+、S2-、CH3COO- |
某兴奋剂的结构简式如图所示.下列说法不正确的是( )


| A、该物质的分子式为C16H16O3 |
| B、该物质分子内所碳原子有可能在同一平面内 |
| C、该物质可发生加成、取代、氧化等反应 |
| D、该物质可使酸性高锰酸钾溶液和溴水褪色,且原理相同 |
下列说法不正确的是( )
A、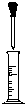 用量筒量取一定量液体时,先从试剂瓶中直接倒入大部分试剂于量筒中,至接近刻度时改用如图所示操作,逐滴加入至刻度 |
| B、金属镁因保存不当造成失火可用细沙盖灭,不能用泡沫灭火器 |
| C、探究温度对化学反应速率影响时,先将硫代硫酸钠与硫酸两种溶液混合后再用水浴加热 |
| D、可用热氢氧化钠溶液鉴别地沟油(餐饮废弃油)和矿物油(汽油、煤油等) |
下列有关实验正确的是( )
A、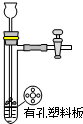 装置用于Na2SO3和浓H2SO4反应制取少量的SO2气体 |
B、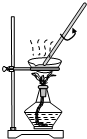 装置用于灼烧CuSO4?5H2O |
C、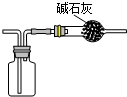 装置用于收集氯气并防止污染空气 |
D、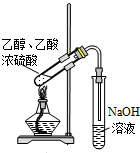 装置用于实验室制备少量乙酸乙酯 |
下列有关说法中,正确的是( )
| A、苯和乙烯都可以使得溴的四氯化碳溶液褪色 |
| B、等物质的量的乙烯和乙醇完全燃烧消耗氧气的量不相等 |
| C、乙醇的酯化反应和酯的水解反应均属于取代反应 |
| D、聚乙烯可以发生加成反应 |
T°C时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X,Y,Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图2所示.下列分析正确的( )
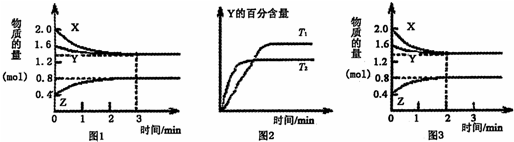

| A、容器中发生的反应可表示为:3X(g)+Y(g)?4Z(g) |
| B、0-3 min内,v(X)=0.2 mol?L-1?min-1 |
| C、若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
| D、其他条件不变升高温度,v正、v重都增大,且重新达到平衡前v正>v重 |
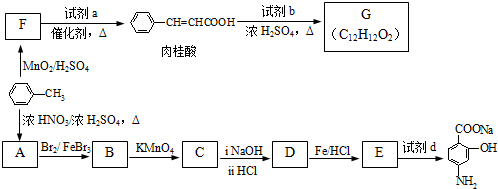
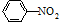
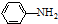
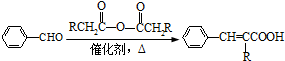 (R=-CH3或-H)
(R=-CH3或-H)