题目内容
7.X2-、Y-、Z3+、W+四种短周期元素微粒具有相同的核外电子层结构,下列叙述正确的是( )| A. | 原子序数X<Y<Z<W | |
| B. | 离子半径X2->Y->Z3+>W+ | |
| C. | 四种元素的最高正价与最低负价绝对值之和均为8 | |
| D. | 原子最外层电子数Y>X>Z>W |
分析 X2-、Y-、Z3+、W+四种短周期元素微粒具有相同的核外电子层结构,则X、Y为位于上一周期的非金属元素,Z、W位于下一周期的金属元素,结合化合价可知,X位于ⅥA族,Y位于ⅤⅡA族,Z位于ⅢA族,W位于第IA族,则X为O,Y为F,Z为Al,W为Na,然后结合元素周期律来解答.
解答 解:X2-、Y-、Z3+、W+四种短周期元素微粒具有相同的核外电子层结构,则X、Y为位于上一周期的非金属元素,Z、W位于下一周期的金属元素,结合化合价可知,X位于ⅥA族,Y位于ⅤⅡA族,Z位于ⅢA族,W位于第IA族,则X为O,Y为F,Z为Al,W为Na,
A.原子序数X<Y<W<Z,故A错误;
B.具有相同电子排布的离子,原子序数大的离子半径小,则离子半径为X2->Y->W+>Z3+,故B错误;
C.X为O,Y为F,没有正价,故C错误;
D.原子最外层电子数为Y(最外层电子数为7)>X(最外层电子数为6)>Z(最外层电子数为3)>W(最外层电子数为1),故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、电子层结构推断元素为解答的关键,侧重分析与应用能力的考查,注意O、F无正价,题目难度不大.

练习册系列答案
相关题目
18.下列化合物中,就有离子键,又有共价键的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | NH3 |
15.据报道,放射性同位素${\;}_{53}^{131}$I 可以治疗肿瘤,该同位素原子核内的中子数为( )
| A. | 53 | B. | 78 | C. | 131 | D. | 125 |
2.工业上合成丁苯橡胶的反应如下(反应条件已略去):
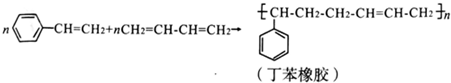
下列有关说法错误的是( )

下列有关说法错误的是( )
| A. | 丁苯橡胶的两种单体都属于烃 | B. | 丁苯橡胶不能使溴水褪色 | ||
| C. | 上述反应的原子利用率为100% | D. | 丁苯橡胶属于高分子化合物 |
12.下列有关放热反应、吸热反应的说法不正确的是( )
| A. | 放热反应放出热量的多少与反应物的质量和状态有关 | |
| B. | 若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应 | |
| C. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| D. | 不管是吸热反应还是放热反应,升高温度,反应速率均增大 |
19.下列离子方程式书写不正确的是( )
| A. | 向CuSO4溶液中加入铁粉:Fe+Cu2+═Cu+Fe2+ | |
| B. | 铁与稀盐酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | 石灰乳与盐酸反应:H++OH-═H2O | |
| D. | 氯化镁溶液与氢氧化钠溶液反应:Mg2++2 OH-═Mg(OH)2↓ |
