题目内容
8.下列做法与可持续发展宗旨相违背的是( )| A. | 加大清洁能源的开发利用,提高资源的利用率 | |
| B. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 | |
| C. | 加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求 | |
| D. | 对工业废水、生活污水净化处理,减少污染物的排放 |
分析 A.加大清洁能源的开发利用,提高资源的利用率,可减少化石能源的利用;
B.利用CO2合成聚碳酸酯类可降解塑料,减少二氧化碳的排放;
C.加大铅酸蓄电池、含汞锌锰干电池的生产,使用后的废弃物影响环境;
D.对工业废水、生活污水净化处理,减少污染物的排放,符合社会可持续发展理念.
解答 解:A.因不可再生能源与可再生能源区别在于能否短期内从自然界得到补充,加大清洁能源的开发利用,如开发太阳能,它是可再生能源,可减少化石能源的利用,减少了二氧化碳、二氧化硫等物质的排放,符合社会可持续发展理念,故A正确;
B.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用应用,减少二氧化碳的排放,符合题意,故B正确;
C.加大铅酸蓄电池、含汞锌锰干电池的生产,废旧电池含有的铅、汞、锌、锰污染和废旧蓄电池电解液污染,会造成污染,不符合社会可持续发展理念,故C错误;
D.水污染主要来自工业、农业、生活污染物的排放,工业废水生活污水经过处理后可以节约资源,保护水源,符合社会可持续发展理念,故D正确;
故选C.
点评 本题考查了化学与生活、社会密切相关知识,主要考查白色污染、清洁能源、绿色化学等知识,掌握常识、理解原因是关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列各物质间的反应,生成的盐不止一种的是( )
| A. | 氧化铁与稀盐酸 | B. | 铜与浓硫酸 | ||
| C. | 钠在氯气中燃烧 | D. | 氯气通入烧碱溶液 |
13.如果向500mL含伪CaCl2和KCl的混合溶液中,加入含1mol碳酸钠的溶液,恰好使钙离子完全沉淀;如果向该溶液中加人含3mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 1mol•L-1 | B. | 2mol•L-1 | C. | 3mol•L-1 | D. | 4mol•L-1 |
3.强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、Al3+、CO32-、SO42-、Cl-中的若干种,某同学为了确认其成分,取溶液X进行连续实验,实验过程及产物如下:

下列结论正确的是( )

下列结论正确的是( )
| A. | X中肯定存在Na+、NH4+、Fe2+、Al3+、SO42- | |
| B. | 气体F经催化氧化可直接生成气体D | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH)3 | |
| D. | X中不能确定的离子是Al3+、Na+、K+和Cl- |
13.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
20.表是元素周期表的一部分.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程: .
.
(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程:
 .
.(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
17.常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )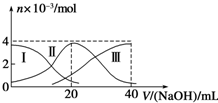

| A. | 等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水大 | |
| B. | 当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| C. | NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) | |
| D. | 向上述加入20mLNaOH溶液后所得溶液中再加入水的过程中,pH可能减少 |