题目内容
15.下列各物质间的反应,生成的盐不止一种的是( )| A. | 氧化铁与稀盐酸 | B. | 铜与浓硫酸 | ||
| C. | 钠在氯气中燃烧 | D. | 氯气通入烧碱溶液 |
分析 A.氧化铁和盐酸反应生成氯化铁溶液;
B.铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
C.钠和氯气反应生成氯化钠;
D.氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
解答 解:A.氧化铁与稀盐酸反应为:Fe2O3+6HCl=2FeCl3+3H2O,生成盐只有一种,故A不符合;
B.铜与浓硫酸加热反应,Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,生成盐只有一种,故B不符合;
C.钠在氯气中燃烧生成氯化钠,2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl,生成盐只有一种,故C不符合;
D.氯气通入烧碱溶液反应生成氯化钠、次氯酸钠和水,Cl2+2NaOH=NaCl+NaClO+H2O,生成盐有两种,故D符合;
故选D.
点评 本题考查了物质性质、产物判断,主要是氧化铁、铜、钠氯气在的熟练掌握,题目难度不大.

练习册系列答案
相关题目
5.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g样品加热,其质量变为w2 g,则该样品的纯度(质量分数)是( )
| A. | $\frac{115{w}_{2}-84{w}_{1}}{31{w}_{1}}$ | B. | $\frac{84({w}_{1}-{w}_{2})}{31{w}_{1}}$ | ||
| C. | $\frac{73{w}_{2}-42{w}_{1}}{31{w}_{1}}$ | D. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ |
3.将四氯化碳加入浓碘水中,碘水的颜色变浅,这是由于发生了( )
| A. | 化学反应 | B. | 取代反应 | C. | 加成反应 | D. | 萃取过程 |
10.为达到下表所列的实验目的,所采用的实验方法正确的是( )
| 实验目的 | 实验方法 | |
| A | 检验某混合溶液中是否有Cl- | 取样滴加AgNO3溶液 |
| B | 检验氯化铵中的NH4+ | 加热后,用湿润的红色石蕊试纸靠近试管口 |
| C | 鉴别CO2和SO2 | 分别通入澄清石灰水 |
| D | 检验某试液中是否含有SO42- | 取样滴入盐酸酸化后,再滴入BaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
20.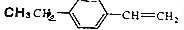 分子中,处于同一平面上的碳原子数最多可能是( )
分子中,处于同一平面上的碳原子数最多可能是( )
 分子中,处于同一平面上的碳原子数最多可能是( )
分子中,处于同一平面上的碳原子数最多可能是( )| A. | 8个 | B. | 9个 | C. | 10个 | D. | 7个 |
7.下列反应中,属于氧化还原反应的是( )
| A. | 2 Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$ Al2O3+3 H2O | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | FeO+2 HCl═FeCl2+H2O | D. | FeCl2+2NaOH═Fe (OH)2↓+2NaCl |
4.已知甲、乙两种烃的含碳的质量分数相同,下列判断正确的是( )
| A. | 甲和乙一定是同分异构体 | B. | 甲和乙的实验式一定相同 | ||
| C. | 甲和乙不可能是同系物 | D. | 甲和乙的分子式一定相同 |
8.下列做法与可持续发展宗旨相违背的是( )
| A. | 加大清洁能源的开发利用,提高资源的利用率 | |
| B. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 | |
| C. | 加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求 | |
| D. | 对工业废水、生活污水净化处理,减少污染物的排放 |
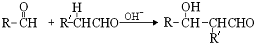
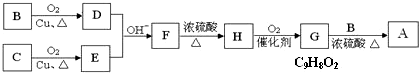
 .
. .
.
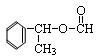 .
.