题目内容
已知450℃,1.0×105Pa时,在有适当催化剂存在下:2SO2(g)+O2(g)═2SO3(g);△H=-Q kJ?mol-1,在相同温度和压强下,向一密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1 kJ,在相同温度和压强下,向另一密闭容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2 kJ,则下列关系中正确的是( )
| A、2Q2=Q1<Q |
| B、2Q2<Q1=Q |
| C、2Q2<Q1<Q |
| D、Q1=2Q2=Q |
考点:反应热的大小比较,反应热和焓变
专题:
分析:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成1molSO3气体放出热量为197kJ,反应为可逆反应,浓度不同,平衡转化的程度不等,根据热化学方程式的含义来分析.
解答:
解:450℃,1.0×105Pa时,在有适当催化剂存在下:2SO2(g)+O2(g)═2SO3(g);△H=-Q kJ?mol-1,由热化学方程式可知,在上述条件下反应生成2molSO3气体放热QkJ,加入2molSO2和1molO2,生成的三氧化硫量小于2mol,所以Q1<Q,在相同温度和压强下,向另一密闭容器中通入1molSO2和0.5molO2,该反应与上述平衡等效,但转化的物质的量为上述一半,所以放出的热量也为上述一半,即<2Q2=Q1,综上得:2Q2=Q1<Q,故选A.
点评:本题考查反应热的计算,题目难度中等,本题注意等效平衡的判断以及可逆反应的特征.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
化学与生产、生活密切相关,下列叙述错误的是( )
| A、用热的纯碱溶液清除灶具上的油污 |
| B、用硫酸清洗锅炉中的水垢 |
| C、用明矾[KAl(SO4)2.12H2O]作净水剂,除去水中悬浮的杂质 |
| D、用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+ |
25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
A、 表示的粒子不会对水的电离平衡产生影响 表示的粒子不会对水的电离平衡产生影响 |
B、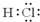 表示的物质加入水中,促进水的电离,c(H+)增大 表示的物质加入水中,促进水的电离,c(H+)增大 |
C、25℃时, 表示的微粒加入水中,促进水的电离,Kw不变 表示的微粒加入水中,促进水的电离,Kw不变 |
| D、水的电离程度只与温度有关,温度越高,电离程度越大 |
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 达平衡时PCl5为0.40mol,如果此时再加入2.0mol PCl3和1.0mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
| A、小于0.40 mol |
| B、大于0.80 mol |
| C、等于0.80 mol |
| D、大于0.40 mol,小于0.80 mol |
下列叙述正确的是( )
| A、用简易量热计能粗略测量稀盐酸和烧碱稀溶液中和反应的反应热 |
| B、pH<7的溶液不可能呈中性 |
| C、所有化学反应的反应热均可通过实验直接测定 |
| D、铅酸蓄电池充电和放电时的所发生的反应互为可逆反应 |
钠元素与硅元素最本质的区别是( )
| A、质子数不同 |
| B、相对原子质量不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
下列反应能用CO32-+2H+═CO2↑+H2O表示的是( )
| A、Na2CO3+H2SO4═Na2SO4+CO2↑+H2O |
| B、CaCO3+2HCl═CaCl2+CO2↑+H2O |
| C、KHCO3+HCl═KCl+CO2↑+H2O |
| D、BaCO3+2HNO3═Ba(NO3 )2+CO2↑+H2O |
