题目内容
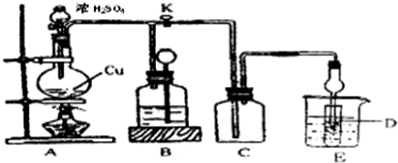
4.A在常温下是一种气体单质,且是最轻的气体;B是一种黄绿色有毒的气体单质;C是一种可以被磁铁吸引的常见金属.回答问题:
(1)写出A、B的名称,A是氢气;B是氯气.
(2)C的元素符号是Fe.
(3)A与B在点燃条件下反应的化学方程式是H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
分析 A在常温下是一种气体单质,且是最轻的气体,则A是氢气,B在常温下是黄绿色气体,则B为Cl2,C是一种可以被磁铁吸引的常见金属铁,由此分析解答.
解答 解:A在常温下是一种气体单质,且是最轻的气体,则A是氢气,B在常温下是黄绿色气体,则B为Cl2,C是一种可以被磁铁吸引的常见金属铁,
(1)A是氢气、B是氯气,故答案为:氢气;氯气;
(2)C是铁,其元素符号是Fe,故答案为:Fe;
(3)氢气与氯气在点燃条件下反应的化学方程式是:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;故答案为:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
点评 本题考查了氯气与氢气的反应,熟悉氯气的性质及氯化氢的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
10.表是元素周期表的一部分.
根据A~G元素在周期表中的位置,用化学式填写空白.
(1)元素中电负性最强的是F,第一电离能最小的是Na.
(2)最高价氧化物对应水化物的酸性最强的酸是HClO4.
(3)D、E、F三种元素按原子半径由大到小的顺序排列为P>N>F.
(4)A的氧化物和B的单质反应后所得溶液的pH>7.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G |
(1)元素中电负性最强的是F,第一电离能最小的是Na.
(2)最高价氧化物对应水化物的酸性最强的酸是HClO4.
(3)D、E、F三种元素按原子半径由大到小的顺序排列为P>N>F.
(4)A的氧化物和B的单质反应后所得溶液的pH>7.
8.某有机物的结构简式如图所示,按官能团分类,它不属于( )


| A. | 烯烃类 | B. | 酚类 | C. | 醚类 | D. | 醇类 |
15.化学与军事及工业生产密切相关,下列说法正确们的是( )
| A. | “歼-2-“飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | ”辽宁舰”上用于舰载机肇落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| C. | 军舰船底镶嵌锌块,可防船体被腐蚀是应用了牺牲阳极的阴极保护法 | |
| D. | 工业上可用氢氟骏与二氧化硅反应进行玻璃雕花,而盐酸不与二氧化硅反立,说明氢氟酸的酸性比盐酸的强 |
9. 工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.某科研小组用该原理处理污水,设计的装置如图所示.下列说法正确的是( )
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.某科研小组用该原理处理污水,设计的装置如图所示.下列说法正确的是( )
 工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.某科研小组用该原理处理污水,设计的装置如图所示.下列说法正确的是( )
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.某科研小组用该原理处理污水,设计的装置如图所示.下列说法正确的是( )| A. | 为了增加污水的导电能力,应向污水中加入适量的H2SO4溶液 | |
| B. | 甲装置中Fe电极的反应为Fe-3e-═Fe3+ | |
| C. | 为了使燃料电池乙长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2 | |
| D. | 当乙装置中有1.6 gCH4参加反应时,C电极理论上生成气体的体积在标况下为4.48 L |
13.在第n层电子层中,当它作为原子的最外电子层时,容纳电子数最多与第(n-1)层相同;当它作为原子的次外电子层时,其电子数比第(n-1)层多10个,则对此电子层的判断正确的是( )
| A. | 必为第1层 | B. | 只能是第2层 | C. | 只能是第3层 | D. | 可以是任意层 |