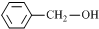题目内容
|
运用有关概念判断下列叙述正确的是 | |
| [ ] | |
A. |
1 mol H2燃烧放出的热量为H2的燃烧热 |
B. |
Na2SO3和H2O2的反应为氧化还原反应 |
C. |
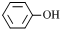
|
D. |
BaSO4的水溶液不导电,故BaSO4是弱电解质 |
答案:B
解析:
解析:
|
该题考查化学反应基本概念.A选项燃烧热的定义是在25℃、101 kPa时,1 moL纯物质完全燃烧生成稳定化合物时所放出的热量,如果生成气态水,就不是H2的燃烧热.所以A选项错误.C选项中两种物质虽然相差-CH2,但前者是酚类物质后者是醇类物质,不符合同系物定义,错误;D选选BaSO4属于盐类,是强电解质,电解质的强弱时指一定条件下能否完全电离的化合物,错误;B选项中Na2SO3具有强还原性,H2O2具有强氧化性,二者能发生氧化还原反应,正确. |

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
 互为同系物
互为同系物 和
和 互为同系物
互为同系物