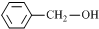题目内容
运用有关概念判断下列叙述正确的是( )
A.1molH2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
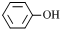
C. 和
和 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
【答案】
B
【解析】燃烧热的概念中除了强调1mol可燃物,还要强调在在25℃、101kPa时完全燃烧,生成稳定的氧化物,H2应该生成H2O(l),而非H2O(g),现在题目未指明状态,A项错误;Na2SO3+H2O2=Na2SO4+H2O是氧化还原反应,B项正确;苯酚与苯甲醇虽官能团均是羟基,但性质不同,种类不同,一个是酚羟基,一个是醇羟基,C项错误;BaSO4难溶于水,故水溶液不导电,但在熔融状态可完全电离而可导电,是强电解质。
【考点定位】本题考查基本概念中的:燃烧热、氧化还原判断、同系物、强弱电解质,需要平时注意区分,在考试时才能正确作答。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 互为同系物
互为同系物