题目内容
13.在合成塔中,点燃氯碱工业产生的气体,可以看到火焰呈苍白色,再用水吸收,可以得到重要的化工原料制盐酸,而工业上生产往往因为含有铁离子而呈现黄色.分析 氯气在氢气中燃烧,火焰由浅兰色变为苍白色,氯化氢溶于水是工业上制盐酸,而工业制盐酸因含铁离子而呈黄色,由此分析解答.
解答 解:氯碱工业产生氢气和氯气,氯气在氢气中燃烧,火焰由浅兰色变为苍白色,氯化氢溶于水是工业上制盐酸,而工业制盐酸因含铁离子而呈黄色,故答案为:苍白;制盐酸;铁离子;黄.
点评 本题考查氯气的性质及氢气在氯气中燃烧的现象,为高频考点,明确反应物与生成物即可解答,题目较简单,注意相关基础知识的积累.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
4.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 78gNa2O2固体中阴离子的个数为2NA | |
| B. | 标准状况1.12L氯气与H2O反应,反应中转移的电子数为0.1NA | |
| C. | CO2通过Na2O2使其增重ag时,反应中转移的电子数为$\frac{a{N}_{A}}{56}$ | |
| D. | 60gSiO2含有的化学键数目为4NA |
1.使用酒精灯时,错误的操作是( )
| A. | 用火柴点燃酒精灯 | |
| B. | 熄灭酒精灯火焰时,用灯帽盖灭 | |
| C. | 用酒精灯外焰给物质加热 | |
| D. | 用燃着的酒精灯去点燃另一盏酒精灯 |
8.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0 L 1.0mol•L-1的KClO4水溶液中含有的氧原子数为4NA | |
| B. | 28g CH3=CH-CH3和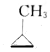 的混合物中所含共用电子对数目为6NA 的混合物中所含共用电子对数目为6NA | |
| C. | 25℃时pH=1的H2SO4溶液中含有H+的数目为0.2NA | |
| D. | 0.1mol 3H37Cl分子中所含中子数为2.3NA |
10.下列关于氯及其化合物说法正确的是( )
| A. | 漂白粉是混合物,有效成分是Ca(ClO)2 | |
| B. | 光照氯水有气泡逸出,该气体是Cl2 | |
| C. | Cl2能使湿润的有色布条褪色,说明Cl2具有漂白性 | |
| D. | 实验室用二氧化锰与稀盐酸反应制取Cl2 |
7.常温下,有一瓶物质是甲和乙的混合物,已知甲和乙的某些性质如下表所示:
据此,将甲和乙相互分离的最佳方法是( )
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 |
| 甲 | -98 | 57.7 | 0.93 | 可溶 |
| 乙 | -84 | 77 | 0.90 | 可溶 |
| A. | 萃取法 | B. | 过滤法 | C. | 蒸馏法 | D. | 分液法 |

 .
.