题目内容
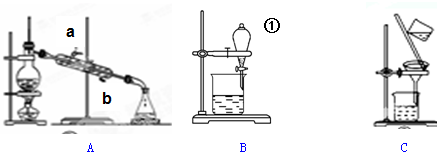
1.使用酒精灯时,错误的操作是( )| A. | 用火柴点燃酒精灯 | |
| B. | 熄灭酒精灯火焰时,用灯帽盖灭 | |
| C. | 用酒精灯外焰给物质加热 | |
| D. | 用燃着的酒精灯去点燃另一盏酒精灯 |
分析 A.酒精灯不能用燃着的酒精灯引燃;
B.熄灭酒精灯火焰时,不能用嘴吹灭;
C.酒精灯外焰温度高;
D.燃着的酒精灯去点燃另一盏酒精灯,易失火.
解答 解:A.酒精灯不能用燃着的酒精灯引燃,可用火柴点燃酒精灯,故A正确;
B.熄灭酒精灯火焰时,不能用嘴吹灭,用灯帽盖灭,故B正确;
C.酒精灯外焰温度高,则用酒精灯外焰给物质加热,故C正确;
D.燃着的酒精灯去点燃另一盏酒精灯,易失火,应火柴点燃酒精灯,故D错误;
故选D.
点评 本题考查化学实验的评价,为高频考点,把握仪器的使用、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验安全及实验评价性分析,题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
12.下列几种说法中正确的是( )
| A. | 摩尔是化学上常用的一个物理量 | |
| B. | 某物质含有6.02×1023个微粒,含有这个数目微粒的物质一定是1 mol | |
| C. | 1摩尔氢气分子可以表示为1 mol H2 | |
| D. | 硫酸的摩尔质量为98 g |
9.关于金属的腐蚀和防护说法不正确的是( )
| A. | 纯的金属在有水的溶液中比不纯的金属(或合金)在其中更容易发生腐蚀 | |
| B. | 金属根据接触的介质的不同,发生腐蚀的化学原理分为:化学腐蚀和电化学腐蚀 | |
| C. | 铝不需要特别的处理就具有抗腐蚀能力 | |
| D. | 在轮船在装上一块锌可以起到保护船身的作用 |
16. 金属及其化合物渗透在生活中的方方面面,其对我们的生活影响很大.
金属及其化合物渗透在生活中的方方面面,其对我们的生活影响很大.
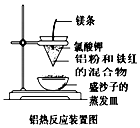
(1)铝热反应可以用于野外焊接钢轨.如图是某同学在实验室中进行
铝热反应(铝过量)的实验装置,实验中他观察到的现象之一为“纸漏斗
的下部被烧穿,有熔融物落入沙中”.
①根据装置图,判断该铝热反应的铝热剂为(写化学式)Al、Fe2O3.
②为定性检验铝热反应后的固体成分,请补充填写下表:
(2)某锂离子电池正极材料含有钴酸锂(LiCoO2),其正极材料可再生利用,其中一步反 应是在加热条件下利用硫酸酸化的双氧水和钴酸锂反应得到CoSO4,写出该反应的化学方程式2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+O2↑+4H2O
(3)纳米铁粉(Fe)可用于处理地下水中的污染物.一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH)4-.
(4)某酸性工业废水中含有有毒的K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+,现有1000L含 21.6mg/L的Cr2O72-溶液,需要27.0g草酸可以完全处理掉Cr2O72-(结果保留3位有效数字).
 金属及其化合物渗透在生活中的方方面面,其对我们的生活影响很大.
金属及其化合物渗透在生活中的方方面面,其对我们的生活影响很大.(1)铝热反应可以用于野外焊接钢轨.如图是某同学在实验室中进行
铝热反应(铝过量)的实验装置,实验中他观察到的现象之一为“纸漏斗
的下部被烧穿,有熔融物落入沙中”.
①根据装置图,判断该铝热反应的铝热剂为(写化学式)Al、Fe2O3.
②为定性检验铝热反应后的固体成分,请补充填写下表:
| 检验成分 | 操作步骤 | 实验现象与相关解释或结论 |
| 铝 | 取少量反应后的固体于试管中,加入足量NaOH溶液,振荡 | ①加入NaOH溶液后,固体部分溶解,用化学方程式解释原因Al2O3+2NaOH=2NaAlO2+H2O ②观察到有气泡产生,证明存在Al. |
| 铁红 | ①另取少量反应后的固体于试管中,加入足量稀硫酸, ②(继续填写后续操作)向试管中滴加KSCN溶液 | ①加入硫酸,固体全部溶解, ②现象为溶液变红色,则证明存在铁红 |
(3)纳米铁粉(Fe)可用于处理地下水中的污染物.一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH)4-.
(4)某酸性工业废水中含有有毒的K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+,现有1000L含 21.6mg/L的Cr2O72-溶液,需要27.0g草酸可以完全处理掉Cr2O72-(结果保留3位有效数字).
6.下列化学反应中,属于氧化还原反应的是( )
| A. | H2SO4+2NaOH═Na2SO4+2H2O | B. | NH3+HCl═NH4Cl | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | Cl2+2NaOH=NaCl+NaClO+H2O |
16.下列说法正确的是( )
| A. | 氢氧燃料电池工作时,1mol H2在正极上失去2mol电子 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的CO32-的数目小于6.02×1022个 | |
| C. | 常温常压下,22.4LCl2中含有的分子数为6.02×1023个 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱 |