题目内容
短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和.
(1)若元素A的某核素的质子数和中子数相等,则该核素的原子组成符号为:
它的最高价氧化物对应的水化物: .
(2)淡黄色固体E的电子式为: .0.2mol的固体E与水反应转移的电子数为 .
(3)用电子式表示C、D两元素形成的化合物C2D的过程 .
(1)若元素A的某核素的质子数和中子数相等,则该核素的原子组成符号为:
它的最高价氧化物对应的水化物:
(2)淡黄色固体E的电子式为:
(3)用电子式表示C、D两元素形成的化合物C2D的过程
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,B的原子序数小于C,则B为O元素、C为Na元素;A的原子序数小于O,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,据此解答.
解答:
解:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,B的原子序数小于C,则B为O元素、C为Na元素;A的原子序数小于O,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,
(1)由上述分析可知,A为C元素,若C的某核素的质子数和中子数相等,则该核素的原子组成符号为:126C,它的最高价氧化物对应的水化物为H2CO3;
故答案为:126C;H2CO3;
(2)淡黄色固体E为Na2O2,属于离子化合物,其电子式为: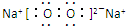 ,2Na2O2+2H2O═4NaOH+O2↑的反应中,只有O元素的化合价发生变化,如果反应了1mol的Na2O2转移的电子的物质的量1mol,则0.2molNa2O2与水完全反应转移电子为0.2NA,
,2Na2O2+2H2O═4NaOH+O2↑的反应中,只有O元素的化合价发生变化,如果反应了1mol的Na2O2转移的电子的物质的量1mol,则0.2molNa2O2与水完全反应转移电子为0.2NA,
故答案为: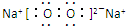 ;0.2NA;
;0.2NA;
(3)C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为: ,
,
故答案为: .
.
(1)由上述分析可知,A为C元素,若C的某核素的质子数和中子数相等,则该核素的原子组成符号为:126C,它的最高价氧化物对应的水化物为H2CO3;
故答案为:126C;H2CO3;
(2)淡黄色固体E为Na2O2,属于离子化合物,其电子式为:
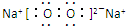 ,2Na2O2+2H2O═4NaOH+O2↑的反应中,只有O元素的化合价发生变化,如果反应了1mol的Na2O2转移的电子的物质的量1mol,则0.2molNa2O2与水完全反应转移电子为0.2NA,
,2Na2O2+2H2O═4NaOH+O2↑的反应中,只有O元素的化合价发生变化,如果反应了1mol的Na2O2转移的电子的物质的量1mol,则0.2molNa2O2与水完全反应转移电子为0.2NA,故答案为:
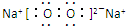 ;0.2NA;
;0.2NA;(3)C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为:
 ,
,故答案为:
 .
.
点评:本题考查结构性质位置关系应用,题目难度中等,根据题干信息正确判断各元素名称为解答关键,试题侧重对常见化学用语的考查,注意对基础知识的积累掌握.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
将含有等体积NH3、CO2、NO的混合气体依次通过盛有浓H2SO4、Na2O2和Na2CO3溶液的装置,充分反应,最后得到的气体是( )
| A、CO2和NO |
| B、CO2 |
| C、NO |
| D、NO2 |
下列各组混合物,可以用分液漏斗分离的是( )
| A、苯和乙醇 | B、乙酸和水 |
| C、溴苯和苯 | D、三氯甲烷和水 |
32g某一元醇跟足量的金属钠完全反应,可以得到11.2L(标准状况)氢气,该醇是( )
| A、CH3OH |
| B、C2H5OH |
| C、C3H7OH |
| D、C4H9OH |
下列仪器中,不能用于加热的是( )
| A、蒸发皿 | B、试管 |
| C、圆底烧瓶 | D、容量瓶 |