题目内容
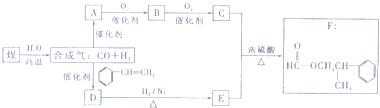
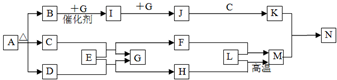
如图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去)其中常温下B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物.N为不溶于水的无机酸.
请回答下列问题:
(1)写出下列物质的化学式
A: F: L:
(2)写出G的一种同素异形体的化学式:
(3)已知工业上生产0.1molB放出4.62kj热量,写出该反应的热化学方程式:
(4)在反应C+E→G+F中,每生成1molG转移 mol电子.

请回答下列问题:
(1)写出下列物质的化学式
A:
(2)写出G的一种同素异形体的化学式:
(3)已知工业上生产0.1molB放出4.62kj热量,写出该反应的热化学方程式:
(4)在反应C+E→G+F中,每生成1molG转移
考点:无机物的推断
专题:推断题
分析:B为气体,可使湿润的红色石蕊试纸变蓝,为NH3,常温下C为无色液体,由A分解生成,C为H2O,由A
NH3+H2O+D,D为气体,故A为碳酸铵或碳酸氢铵,D为CO2;由转化关系NH3
I
J,J能与水反应,G是气体单质,故G为O2,I为NO,J为NO2,K为HNO3;C、D都能与E生成氧气,故E为Na2O2,F为NaOH,H为Na2CO3,N为不溶于水的无机酸,为H2SiO3,由HNO3+M→H2SiO3,可知M为硅酸盐,由氢氧化钠与碳酸钠都能与L反应生成M,故L为SiO2,据此答题.
| G |
| G |
| G |
解答:
解:B为气体,可使湿润的红色石蕊试纸变蓝,为NH3,常温下C为无色液体,由A分解生成,C为H2O,由A
NH3+H2O+D,D为气体,故A为碳酸铵或碳酸氢铵,D为CO2;由转化关系NH3
I
J,J能与水反应,G是气体单质,故G为O2,I为NO,J为NO2,K为HNO3;C、D都能与E生成氧气,故E为Na2O2,F为NaOH,H为Na2CO3,N为不溶于水的无机酸,为H2SiO3,由HNO3+M→H2SiO3,可知M为硅酸盐,由氢氧化钠与碳酸钠都能与L反应生成M,故L为SiO2,
(1)上述分析判断A为NH4HCO3或(NH4)2CO3,F为NaOH,L为SiO2,故答案为:NH4HCO3或(NH4)2CO3;NaOH;SiO2;
(2)O2的一种同素异形体是O3,故答案为:O3;
(3)生成0.1molNH3放出4.62kJ热量,生成氨气的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4k J?mol-1;
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.4k J?mol-1;
(4)在反应2Na2O2+2H2O=4NaOH+O2↑中,Na2O2即使氧化剂又是还原剂,各占一半,每生成1molO2转移电子的物质的量为1mol×2=2mol,故答案为:2.
| G |
| G |
| G |
(1)上述分析判断A为NH4HCO3或(NH4)2CO3,F为NaOH,L为SiO2,故答案为:NH4HCO3或(NH4)2CO3;NaOH;SiO2;
(2)O2的一种同素异形体是O3,故答案为:O3;
(3)生成0.1molNH3放出4.62kJ热量,生成氨气的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4k J?mol-1;
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.4k J?mol-1;
(4)在反应2Na2O2+2H2O=4NaOH+O2↑中,Na2O2即使氧化剂又是还原剂,各占一半,每生成1molO2转移电子的物质的量为1mol×2=2mol,故答案为:2.
点评:本题考查无机物的推断,B及I的连续氧化,C与D的转化为解答本题的突破口,利用转化推断出各物质是解答本题的关键,题目难度中等.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
下列物品的盛放错误的是( )
| A、过氧化钾固体必须密封保存 |
| B、烧碱必须密封保存 |
| C、碱金属必须保持在煤油中 |
| D、氢氧化钠溶液用带玻璃塞的玻璃瓶存放 |
向饱和Na2CO3溶液中通入足量CO2,下列说法不正确的是( )
| A、溶液中有Na2CO3?10H2O晶体析出 |
| B、溶液中的PH减小 |
| C、溶液中发生的离子反应为:CO2+H2O+CO32-═2HCO3- |
| D、溶液中Na+的物质的量减少 |
下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
| A、碘水 | B、溴水 |
| C、氯水 | D、NaOH溶液 |
将过氧化钠和过量的碳酸氢钠在密闭容器中混合充分加热后,最终残留固体物质是( )
| A、Na2CO3 |
| B、Na2O和Na2O2 |
| C、Na2O2 |
| D、Na2O2和Na2CO3 |