题目内容
2013年2月1日上午9时许,连霍高速义昌大桥上一辆装载烟花炮竹的货车发生爆炸,导致大桥垮塌,造成重大损失.制作烟花炮竹需要硝酸钾,下列关于硝酸钾的叙述不正确的是( )
| A、是一种盐 |
| B、化学式KNO3 |
| C、摩尔质量为101g |
| D、难以发生复分解反应 |
考点:酸、碱、盐、氧化物的概念及其相互联系,摩尔质量
专题:物质的分类专题,阿伏加德罗常数和阿伏加德罗定律
分析:硝酸钾的化学式为KNO3,由酸根离子和钾离子构成属于盐,在溶液中不容易反应,其摩尔质量为101g/mol,据此分析.
解答:
解:A、KNO3由酸根离子和钾离子构成属于盐,故A正确;
B、硝酸钾的化学式为KNO3,故B正确;
C、摩尔质量的单位不是g,硝酸钾的摩尔质量为101g/mol,故C错误;
D、KNO3在溶液中电离出钾离子和硝酸根离子,二者与其它离子不容易生成沉淀,难以发生复分解反应,故D正确.
故选C.
B、硝酸钾的化学式为KNO3,故B正确;
C、摩尔质量的单位不是g,硝酸钾的摩尔质量为101g/mol,故C错误;
D、KNO3在溶液中电离出钾离子和硝酸根离子,二者与其它离子不容易生成沉淀,难以发生复分解反应,故D正确.
故选C.
点评:本题考查了物质的分类和物质的性质,注意把握盐的概念,根据物质的构成分析,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O═7X+5FeSO4+12H2SO4,下列说法正确的是( )
| A、X的化学式为CuS,它既是氧化产物又是还原产物 |
| B、5 mol FeS2发生反应,有10 mol电子转移 |
| C、产物中的SO42-离子有一部分是氧化产物 |
| D、FeS2只作还原剂 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1molCl2与足量的氢氧化钠溶液反应转移的电子数为0.2 NA |
| B、12.5mL 16mol/L浓硫酸与足量铜反应,转移的电子数为0.2NA |
| C、6.2g氧化钠和7.8g过氧化钠中所含有的离子数均为0.3 NA |
| D、2.24L氯气与氢氧化钠溶液完全反应转移的电子数为0.1 NA |
下列反应的离子方程式中,书写正确的是( )
| A、石英溶于氢氧化钠溶液:SiO2+2OH-═SiO32-+H2O |
| B、将铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、铁粉与硫酸铁溶液反应:Fe+Fe3+═2Fe2+ |
| D、金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物.下列生产乙醇的反应中,原子利用率最高的是( )
A、乙烯水化:CH2=CH2+H2O
| |||
B、葡萄糖发酵:C6H12O6
| |||
C、溴乙烷水解:CH3CH2Br+H2O
| |||
D、丙酸乙酯水解:CH3CH2COOCH2CH3+H2O
|
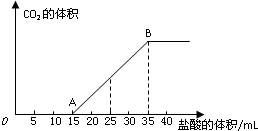 将一定体积的CO2通入到50mL某浓度的NaOH溶液中,得到溶液甲.为了测定其溶液甲的成分,向该溶液甲中加入1mol/L的盐酸,所加入的盐酸与产生CO2的体积(标况)的关系如图所示:
将一定体积的CO2通入到50mL某浓度的NaOH溶液中,得到溶液甲.为了测定其溶液甲的成分,向该溶液甲中加入1mol/L的盐酸,所加入的盐酸与产生CO2的体积(标况)的关系如图所示: