题目内容
19.下列化合物的电子式书写正确的是( )| A. |  | B. |  | C. | 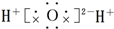 | D. | 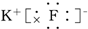 |
分析 A、氯化钙为离子化合物,阴离子个数不能合并;
B、次氯酸中O分别与H和Cl形成一对共价键;
C、水为共价化合物,不能用括号;
D.KF为离子化合物,阴离子需要括号,且标明所带电荷数.
解答 解:A、氯化钙电子式为 ,故A错误;
,故A错误;
B、氯原子最外层7个电子成1个共价键、氧原子的最外层6个电子,成2个共价键,电子式为 ,故B错误;
,故B错误;
C、过氧化氢是共价化合物,不存在离子键,氧原子之间形成1对共用电子对,氢原子与氧原子之间形成1对共用电子对,电子式为 ,故C错误;
,故C错误;
D、氟化钾为离子化合物,电子式为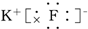 ,书写正确,故D正确,
,书写正确,故D正确,
故选D.
点评 本题考查电子式的书写,难度不大,注意电子式中的电子数是指最外层电子数,而不是指电子总数.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
9.已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ,则氢气中1molH-H键断裂时吸收热量为 ( )
| A. | 872kJ | B. | 557kJ | C. | 436kJ | D. | 188kJ |
10.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数K=1.44 | |
| D. | 其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大 |
14.化学于生产、生活,并应用于生产、生活,下列有关说法不正确的是( )
| A. | 明矾能水解生成氢氧化铝胶体,可用作净水剂 | |
| B. | 石英、玛瑙、水晶通常作为装饰品使用,但都可溶于氢氟酸 | |
| C. | Na2CO3俗称纯碱,可与盐酸反应,故可用于治疗人体内胃酸过多 | |
| D. | 农村施肥时,草木灰不能与铵态氮肥混用,以免氮肥肥效下降 |
4.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑦七种元素在周期表中的位置.
请回答:
(1)下列元素分别是①Na(填元素符号,下同),其中化学性质最不活泼的是Ar.
(2)⑥元素的氢化物是 (填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(3)⑦元素与①元素形成的化合物是NaC(填化学式),高温下灼烧该化合物时,火焰呈黄色.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | ④ | ||||
| 4 | ② |
(1)下列元素分别是①Na(填元素符号,下同),其中化学性质最不活泼的是Ar.
(2)⑥元素的氢化物是
 (填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.(3)⑦元素与①元素形成的化合物是NaC(填化学式),高温下灼烧该化合物时,火焰呈黄色.
11.化学与生产、生活、社会密切相关.下列有关说法中正确的是( )
| A. | 2008年北京奥运会开幕式上的“脚印”等焰火让全世界为之欢呼、倾倒,这主要是利用了“焰色反应”这一化学反应放出的能量 | |
| B. | 食盐中因为含有少量CaCl2、MgCl2晶体易潮解,它们潮解的实质是晶体表面吸水形成溶液 | |
| C. | 2013年11月,中科院国家纳米科学中心首次“拍”到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| D. | 神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型有机高分子材料 |
8.下列分子中所有原子都满足最外层8电子结构的是( )
①光气(COCl2) ②六氟化硫 ③HCHO ④三氟化硼 ⑤PCl3 ⑥PCl5 ⑦NO2 ⑧二氟化氙 ⑨N2 ⑩CH4.
①光气(COCl2) ②六氟化硫 ③HCHO ④三氟化硼 ⑤PCl3 ⑥PCl5 ⑦NO2 ⑧二氟化氙 ⑨N2 ⑩CH4.
| A. | ⑥⑦⑨ | B. | ①⑤⑨ | C. | ①④⑤⑦ | D. | ①④⑤⑨ |