题目内容
下列说法中正确的是( )
| A、在氧化还原反应中,一定是一种元素被氧化,另一种元素被还原 |
| B、在氧化还原反应中,不一定所有元素的化合价都发生改变 |
| C、氧化还原反应的实质是元素化合价的升降 |
| D、某元素由化合态转化为游离态,这种元素一定被还原了 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应的实质为电子的转移,特征是元素化合价的升降,氧化还原反应可发生在相同元素之间,也可在不同元素之间,结合元素化合价的变化解答该题.
解答:
解:A.氧化还原反应可发生在相同元素之间,如氯气和水、NaOH的反应,只有Cl元素化合价的变化,故A错误;
B.在氧化还原反应中,不一定所有元素的化合价都发生改变,如Cl2+H2O=HCl+HClO,氢元素和氧元素化合价均未变,故B正确;
C.氧化还原反应的实质是电子的转移,故C错误;
D.元素由化合态转化为游离态时,化合价可能升高也可能降低,该元素可能被还原也可能被氧化,故D错误.
故选B.
B.在氧化还原反应中,不一定所有元素的化合价都发生改变,如Cl2+H2O=HCl+HClO,氢元素和氧元素化合价均未变,故B正确;
C.氧化还原反应的实质是电子的转移,故C错误;
D.元素由化合态转化为游离态时,化合价可能升高也可能降低,该元素可能被还原也可能被氧化,故D错误.
故选B.
点评:本题考查学生氧化还原反应的基本概念知识,为高频考点,侧重于概念的理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
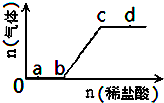 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列粒子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列粒子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:Na+、SO42-、NO3-、Fe(OH)3胶体微粒 |
| B、b点对应的溶液中:Al3+、H+、MnO4-、Cl- |
| C、c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D、d点对应的溶液中:F-、NO3-、Fe2+、Ag+ |
下列说法正确的是( )
| A、氢氧燃料电池的能量转换形式之一为化学能转化为电能 |
| B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C、电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
| D、催化剂通过降低化学反应的焓变加快化学反应速率 |
下列各组离子在指定溶液中,一定能大量共存的是( )
| A、加入KSCN显红色的溶液中:Na+、Cu2+、Cl-、I- |
| B、c(CO32-)=0.1mol/L的溶液中:K+、Na+、Cl-、I- |
| C、c(H+)/c(OH-)=1012的溶液中:NH4+、Fe2+、NO3-、SO42- |
| D、甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
99℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,下列叙述不正确的是( )
| A、此时水的离子积KW=1×10-12 |
| B、水电离出的c(H+)=1×10-12mol.L-1), |
| C、水的电离程度随温度升高而增大 |
| D、c(Na+)=c(SO42-) |
若用NA表示阿伏伽德罗常数的值,则下列说法错误的是( )
| A、71gCl2变为Cl-可失去2NA个电子 |
| B、标准状况下1molN2和SO2的混合物的体积约占22.4L |
| C、NA个O2和NA个H2的质量比为16:1 |
| D、常温常压下4g氦气含NA个氦原子 |
下列说法正确的是( )
| A、35Cl和37Cl互为同素异形体 | ||||
| B、O2和O3是氧元素的两种同位素 | ||||
| C、35Cl和37Cl中35、37表示的是质量数 | ||||
D、1
|
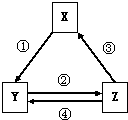 下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )