题目内容
【题目】下列说法不正确的是( )
A. 某试样焰色反应呈黄色,则试样中一定不含有![]()
B. 鉴别![]() 和
和![]() 溶液可用硝酸酸化的硝酸银溶液
溶液可用硝酸酸化的硝酸银溶液
C. 容量瓶不能用作溶解物质的容器
D. 粗盐的提纯实验中,滤液在蒸发皿中加热蒸发结晶
【答案】A
【解析】
A.据试样焰色呈黄色,说明样品中含有钠元素,要确定是否含有钾元素,还要透过蓝色钴玻璃,A项错误;
B.向NaCl和KI溶液中,加入硝酸酸化的硝酸银溶液,产生白色沉淀的是氯化钠,产生黄色沉淀的是KI溶液,B项正确;
C.容量瓶唯一的作用是用来确定一个精确的溶液的体积,既不能用作反应的容器,也不能用作溶解、稀释、贮存的容器等,C项错误;
D.粗盐提纯实验中,蒸发操作使用蒸发皿来盛装滤液进行直接加热,D项正确;
所以答案选择A项。

【题目】甲醇是一种可再生能源,具有广阔的开发和应用前景,可用Pt/Al2O3、Pd/C、 Rh/SiO2等作催化剂,采用如下反应来合成甲醇:2H2 (g)+CO(g)CH3OH(g)
(1)下表所列数据是各化学键的键能,该反应的ΔH=_______(用含字母的代数式表示)。
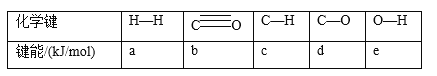
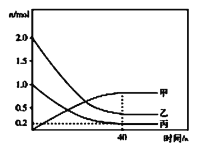
(2)某科研小组用Pd/C作催化剂,在450℃时,研究了n(H):n(CO)分别为2:1、3:1时CO转化率的变化情况(如图),则图中表示n(H2):n(CO)=3:1的变化曲线为______(填“曲线a"或“曲线b”)。
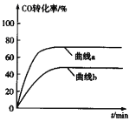
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在2L的恒容密闭容器内充入1 mol CO和2molH2,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20min时,CO的平均反应速率为________,该温度下的平衡常数K为_______.
(4)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g) CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。
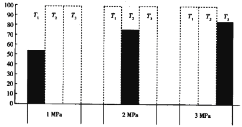
T1、T2、T3由大到小的关系是_________,判断理由是____________
(5)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图
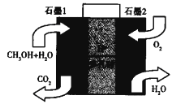
①石墨2为__________ (填“正“或“负“)极。
②石墨1极发生的电极反应式为________