题目内容
苯甲酸在制药和化工行业有着广泛应用,某同学在实验室尝试用甲苯制备苯甲酸.反应原理如下:
C6H5-CH3+2KMnO4→C6H5-COOK+KOH+2MnO2↓+H2O
C6H5-COOK+HCl
C6H5-COOH+KCl
制备过程:将一定量甲苯和KMnO4溶液在100℃反应一段时间后停止反应,对反应混合物进行如图操作:
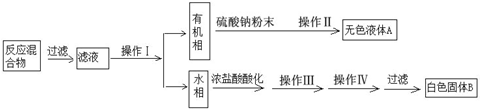
查阅资料得知:苯甲酸的熔点为122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g.
(1)操作Ⅰ、Ⅱ、Ⅲ、Ⅳ的名称分别是 、 、 、 .
(2)硫酸钠粉末的作用是 .
(3)定性检验无色液体A的试剂是 ,现象是 .
(4)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物.为检验是否含KCl,取少量白色固体溶于水,过滤后需向滤液中加入的试剂是 .
(5)为测定白色固体B的纯度,称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol.则固体B中苯甲酸的质量分数为 (保留三位有效数字).
C6H5-CH3+2KMnO4→C6H5-COOK+KOH+2MnO2↓+H2O
C6H5-COOK+HCl
| △ |
制备过程:将一定量甲苯和KMnO4溶液在100℃反应一段时间后停止反应,对反应混合物进行如图操作:

查阅资料得知:苯甲酸的熔点为122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g.
(1)操作Ⅰ、Ⅱ、Ⅲ、Ⅳ的名称分别是
(2)硫酸钠粉末的作用是
(3)定性检验无色液体A的试剂是
(4)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物.为检验是否含KCl,取少量白色固体溶于水,过滤后需向滤液中加入的试剂是
(5)为测定白色固体B的纯度,称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol.则固体B中苯甲酸的质量分数为
考点:物质分离和提纯的方法和基本操作综合应用,探究物质的组成或测量物质的含量
专题:实验设计题
分析:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按流程分离出苯甲酸和回收未反应的甲苯;具体流程为甲苯和KMnO4溶液在100℃反应,则生成了苯甲酸钾、二氧化锰和水,过滤除去二氧化锰,滤液则含有苯甲酸钾的混合溶液经过操作Ⅰ,分成有机相和水相,所以操作Ⅰ为分液;有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯,所以操作Ⅱ为蒸馏;水相主要是苯甲酸钾的水溶液,用浓盐酸酸化生成苯甲酸的溶液经过操作Ⅲ和操作Ⅳ,再过滤得到白色固体B即苯甲酸,所以操作Ⅲ和操作Ⅳ分别为蒸发浓缩、冷却结晶,
(1)依据流程分析混合物分离的实验方法和操作步骤;
(2)有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯来分析;
(3)依据分离试剂和过程可知,有机相中主要是为反应的甲苯,甲苯是苯的同系物,可以被高锰酸钾溶液氧化;
(4)根据AgNO3溶液和稀HNO3来检验氯离子分析;
(5)称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,注意溶液体积变化计算样品中苯甲酸的物质的量,计算质量分数.
(1)依据流程分析混合物分离的实验方法和操作步骤;
(2)有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯来分析;
(3)依据分离试剂和过程可知,有机相中主要是为反应的甲苯,甲苯是苯的同系物,可以被高锰酸钾溶液氧化;
(4)根据AgNO3溶液和稀HNO3来检验氯离子分析;
(5)称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,注意溶液体积变化计算样品中苯甲酸的物质的量,计算质量分数.
解答:
解:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按流程分离出苯甲酸和回收未反应的甲苯,具体流程为甲苯和KMnO4溶液在100℃反应,则生成了苯甲酸钾、二氧化锰和水,过滤除去二氧化锰,滤液则含有苯甲酸钾的混合溶液经过操作Ⅰ,分成有机相和水相,所以操作Ⅰ为分液;有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯,所以操作Ⅱ为蒸馏;水相主要是苯甲酸钾的水溶液,用浓盐酸酸化生成苯甲酸的溶液经过操作Ⅲ和操作Ⅳ,再过滤得到白色固体B即苯甲酸,所以操作Ⅲ和操作Ⅳ分别为蒸发浓缩、冷却结晶,
(1)根据以上分析,所以操作Ⅰ是分离出有机相甲苯,用分液方法得到;操作Ⅱ是蒸馏的方法控制甲苯沸点得到纯净的甲苯液体;苯甲酸的溶液经过操作Ⅲ和操作Ⅳ,再过滤得到白色固体B即苯甲酸,所以操作Ⅲ和操作Ⅳ分别为蒸发浓缩、冷却结晶,故答案为:分液,蒸馏,蒸发浓缩,冷却结晶;
(2)有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯,所以硫酸钠粉末的作用是干燥(或除水),
故答案为:干燥(或除水);
(3)依据流程和推断可知,无色液体A为甲苯,检验试剂可以用酸性高锰酸钾溶液,甲苯被氧化为苯甲酸,高锰酸钾溶液紫色褪去;
故答案为:酸性KMnO4溶液,紫色溶液褪色;
(4)因为加入AgNO3溶液和稀HNO3,如果能生成白色沉淀,则证明溶液中含有氯离子,否则没有,故答案为:AgNO3溶液和稀HNO3;
(5)称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,则样品中苯甲酸质量分数=
×100%=87.1%;
故答案为:87.1%.
(1)根据以上分析,所以操作Ⅰ是分离出有机相甲苯,用分液方法得到;操作Ⅱ是蒸馏的方法控制甲苯沸点得到纯净的甲苯液体;苯甲酸的溶液经过操作Ⅲ和操作Ⅳ,再过滤得到白色固体B即苯甲酸,所以操作Ⅲ和操作Ⅳ分别为蒸发浓缩、冷却结晶,故答案为:分液,蒸馏,蒸发浓缩,冷却结晶;
(2)有机相加碳酸钠粉末吸收有机物中少量的水,再经过操作Ⅱ得到无水液体A即为有机物甲苯,所以硫酸钠粉末的作用是干燥(或除水),
故答案为:干燥(或除水);
(3)依据流程和推断可知,无色液体A为甲苯,检验试剂可以用酸性高锰酸钾溶液,甲苯被氧化为苯甲酸,高锰酸钾溶液紫色褪去;
故答案为:酸性KMnO4溶液,紫色溶液褪色;
(4)因为加入AgNO3溶液和稀HNO3,如果能生成白色沉淀,则证明溶液中含有氯离子,否则没有,故答案为:AgNO3溶液和稀HNO3;
(5)称取1.4g该固体溶于甲醇配成100mL溶液.移取25mL溶液于锥形瓶中,滴入KOH溶液至恰好完全反应,消耗KOH的物质的量为2.5×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,则样品中苯甲酸质量分数=
| 2.5×10 -3mol×4×122g/mol |
| 1.4g |
故答案为:87.1%.
点评:本题考查了物质性质的实验分析判断,物质分离条件,试剂选择,操作步骤的理解应用,物质成分的实验设计方案、步骤、试剂,样品纯度的计算,题目难度中等.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
下列反应中,有沉淀产生且不会消失的是( )
| A、向NaOH溶液中逐滴滴入Fe2(SO4)3溶液直至过量 |
| B、将NaOH溶液逐滴滴入AlCl3溶液中,直至过量 |
| C、向AlCl3溶液中逐滴滴入稀硫酸 |
| D、将氨水逐滴滴入硝酸银溶液中,直至过量 |
下列叙述正确的是( )
| A、同温同压下,物质的物质的量相等,其体积一定相同 |
| B、等体积的二氧化碳和一氧化碳所含的分子数一定相等 |
| C、1L氮气一定比1L氧气的质量小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等 |
A、B、C、D、E是同一周期的五种主族元素,A与B的最高氧化物对应的水化物呈碱性,且碱性B>A;C和D的气态氢化物稳定性为C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序为( )
| A、ABCDE |
| B、CDABE |
| C、BADCE |
| D、ECDBA |
0.75molRO32- 共有30mol电子,则R在元素周期表中的位置是( )
| A、.第二周期ⅤA族 |
| B、.第三周期ⅣA族 |
| C、.第二周期ⅥA族 |
| D、.第三周期Ⅶ族 |
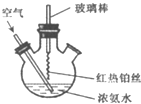
在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通人空气,将红热的铂丝插人瓶中并接近液面.反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热.下列有关说法错误的是( )

| A、反应后溶液中含有NO3- |
| B、反应后溶液中c(H+)增大 |
| C、实验过程中有化合反应发生 |
| D、实验过程中NH3?H2O的电离常数不可能发生变化 |